一碳化学是以分子中只含一个碳原子的化合物为原料生产化工产品的方法。合成气(CO和H2的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
Ⅰ:C(s)+H2O(g)⇌CO(g)+H2(g)
Ⅱ:CO(g)+H2O(g)⇌CO2(g)+H2(g)
Ⅲ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
(1)当反应Ⅰ达到平衡后,下列措施可提高正反应速率的是 ACAC。
A.通入H2O
B.加入焦炭
C.升高温度
D.分离出氢气
(2)若在恒温恒容容器中仅发生反应Ⅰ,则下列不能说明反应达到平衡状态的是 CDCD。
A.容器内气体的压强不变
B.容器内气体的密度不变
C.v(H2O)=v(CO)
D.单位时间内,1molO-H键断裂,同时有1molH-H键断裂
(3)在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应Ⅲ。
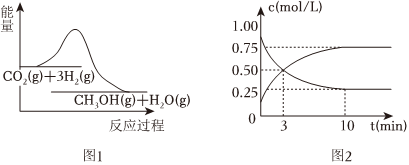
①图1表示该反应进行过程中能量的变化,则该反应是 放热放热(填“吸热”或“放热”)反应。
②反应过程中测得CO2和CH3OH(g)的浓度随时间变化如图2所示。3min时的正反应速率 >>(填“>”,“=”或“<”)逆反应速率,从反应开始到第10min,氢气的平均反应速率v(H2)=0.225mol/(L•min)0.225mol/(L•min)。
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质溶液为稀硫酸的氢氧燃料电池原理示意图,试回答下列问题:
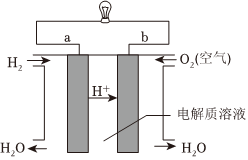
①b为电池的 正正(填“正”或“负”)极。
②a的电极方程式 2H2-2e-=2H+2H2-2e-=2H+。
【答案】AC;CD;放热;>;0.225mol/(L•min);正;2H2-2e-=2H+
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/26 8:0:9组卷:31引用:1难度:0.6
相似题
-
1.氢气最早于16世纪被人工制取出来,氢气是一种清洁能源。
(1)利用光伏电池电解水制H2是氢能的重要来源。已知:H-H键、O=O键、H-O键的键能依次为436kJ•mol-1、495kJ•mol-1、463kJ•mol-1。则2H2O(g)═2H2(g)+O2(g)△H=kJ•mol-1。
(2)T1℃时,向5L恒容密闭容器中充入0.5molCH4,只发生反应2CH4(g)⇌C2H4(g)+2H2(g),达到平衡时,测得c(C2H4)=2c(CH4),CH4的转化率为;保持其他条件不变,温度改为T2℃,经25s后达到平衡,测得c(CH4)=2c(C2H4),则0~25s内v(C2H4)=mol•L-1•s-1。
(3)CH4分解时几种气体的平衡分压(pPa)的对数值lgp与温度的关系如图所示。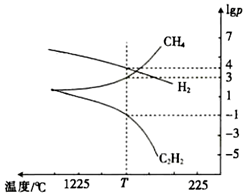
①T℃时,向一恒容密闭容器中通入一定量的CH4(g)、C2H4(g)和H2(g),只发生反应2CH4(g)⇌C2H2(g)+3H2(g)ΔH,ΔH(填“>”或“<”)0,此时的平衡常数Kp=(用平衡分压代替浓度进行计算)Pa2。
②若只改变一个反应条件使Kp变大,则该条件是(填标号)。
A.减小C2H2的浓度
B.升高温度
C.增大压强
D.加入合适的催化剂
(4)工业上,以KNH2和液氨为电解质,以石墨为电极,电解液氨制备H2。阳极的电极反应式为,一段时间后阴、阳两极收集到的气体质量之比为。发布:2025/1/4 8:0:1组卷:9引用:3难度:0.5 -
2.反应 4A(g)+5B(g)⇌4C(g)+6D(g)在 5L 的密闭容器中进行,半分钟后,C 的物质的量增 加了 0.30mol。下列叙述正确的是( )
发布:2024/12/30 19:30:2组卷:67引用:6难度:0.6 -
3.将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1mol/(L•min).求:
(1)此时A的浓度c(A)=mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)=mol;
(2)B的平均反应速率v(B)=mol/(L•min);
(3)x的值为.发布:2024/12/30 19:0:1组卷:164引用:26难度:0.3


