乙苯被吸附在催化剂表面发生脱氢可生成苯乙烯、苯甲醛等,生成苯乙烯的相关反应如下。
反应1:C6H5CH2CH3(g) C6H5CH=CH2(g)+H2(g) ΔH1=117.6kJ•mol-1
反应2:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=41.2kJ•mol-1
反应3:2H2(g)+O2(g) 2H2O(g) ΔH3=-483.6kJ•mol-1
(1)反应4:C6H5CH2CH3(g)+12O2(g) C6H5CH=CH2(g)+H2O(g) ΔH4=-124.2-124.2kJ•mol-1。
(2)较低温度下,向乙苯脱氢的反应体系中加入少量O2,乙苯平衡转化率较高而苯乙烯的选择性较低,其原因可能是 加入少量O2,H2与O2反应放热,氢气浓度减小和体系温度升高都使反应1平衡右移使乙苯转化率升高,但温度升高,苯乙烯(或乙苯)被进一步氧化成苯乙醛等副产物加入少量O2,H2与O2反应放热,氢气浓度减小和体系温度升高都使反应1平衡右移使乙苯转化率升高,但温度升高,苯乙烯(或乙苯)被进一步氧化成苯乙醛等副产物。
(3)向乙苯脱氢反应体系中加入CO2,乙苯转化率与体系中CO2分压强的关系如题图1所示。随CO2的增加,乙苯转化率先增大后减小的可能原因为 前一阶段,随着CO2分压强增大,反应2的平衡正向移动,降低了c(H2),促进反应1正向进行,使乙苯转化率增大,当CO2分压强过大多时,CO2占据了催化剂表面,使催化剂表面吸附的乙苯减少,乙苯转化率下降前一阶段,随着CO2分压强增大,反应2的平衡正向移动,降低了c(H2),促进反应1正向进行,使乙苯转化率增大,当CO2分压强过大多时,CO2占据了催化剂表面,使催化剂表面吸附的乙苯减少,乙苯转化率下降。

(4)研究发现在V2O5/MgO催化剂表面进行CO2的乙苯脱氢反应中,V(+5价)是反应的活性中心,转化过程如题图2所示。
①转化Ⅰ发生反应的化学方程式为 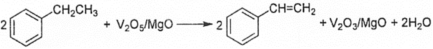
 。反应一段时间后,催化剂活性有所下降,原因可能有反应过程产生的积碳覆盖在活性中心表面和 催化剂中V(+5价)的含量减少催化剂中V(+5价)的含量减少。
。反应一段时间后,催化剂活性有所下降,原因可能有反应过程产生的积碳覆盖在活性中心表面和 催化剂中V(+5价)的含量减少催化剂中V(+5价)的含量减少。
②简述转化Ⅱ的作用 将V2O3转化为V2O5,使催化剂获得再生,同时可以消除积碳将V2O3转化为V2O5,使催化剂获得再生,同时可以消除积碳。
③CO2参与的乙苯脱氢机理如题图3所示(α、β表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,B1、B2位点带部分负电荷)。

1
2


【考点】用盖斯定律进行有关反应热的计算;化学平衡的影响因素.
【答案】-124.2;加入少量O2,H2与O2反应放热,氢气浓度减小和体系温度升高都使反应1平衡右移使乙苯转化率升高,但温度升高,苯乙烯(或乙苯)被进一步氧化成苯乙醛等副产物;前一阶段,随着CO2分压强增大,反应2的平衡正向移动,降低了c(H2),促进反应1正向进行,使乙苯转化率增大,当CO2分压强过大多时,CO2占据了催化剂表面,使催化剂表面吸附的乙苯减少,乙苯转化率下降; ;催化剂中V(+5价)的含量减少;将V2O3转化为V2O5,使催化剂获得再生,同时可以消除积碳
;催化剂中V(+5价)的含量减少;将V2O3转化为V2O5,使催化剂获得再生,同时可以消除积碳
 ;催化剂中V(+5价)的含量减少;将V2O3转化为V2O5,使催化剂获得再生,同时可以消除积碳
;催化剂中V(+5价)的含量减少;将V2O3转化为V2O5,使催化剂获得再生,同时可以消除积碳【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/9 5:0:8组卷:30引用:1难度:0.7
相似题
-
 1.第五主族的磷单质及其化合物在工业上有广泛应用.
1.第五主族的磷单质及其化合物在工业上有广泛应用.
(1)同磷灰石在高温下制备黄磷的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)△H已知相同条件下:4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H12Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g)△H2SiO2(s)+CaO(s)=CaSiO3(s)△H3用△H1、△H2和△H3表示△H,则△H=;
(2)白磷与氧气反应生成P4O10固体.已知断裂下列化学键需要吸收的能量分别为:P-P a kJ•mol-1、P-O b kJ•mol-1、P═O c kJ•mol-1、O═O d kJ•mol-1.根据图1的分子结构和有关数据通过计算写出该反应的热化学方程式为.
(3)三聚磷酸可视为三个磷酸分子(磷酸结构式如图2)之间脱去两个水分子产物,其结构式为,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为.
(4)次磷酸(H3PO2)为一元酸,分子中含一个羟基,其钠盐的正盐的化学式为,该盐可用于工业上的化学镀镍.①化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性等条件下发生下述反应:
(a)□Ni2++□H2PO2-+□=□Ni++□H2PO3-+□
(b)6H2PO-2+2H+=2P+4H2PO3-+3H2↑请在答题卡上写出并配平反应式(a);
②利用①中反应可在塑料镀件表面沉积镍-磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀.请从以下方面比较化学镀与电镀.原理上的不同点:;化学镀的优点:.发布:2024/11/19 8:0:1组卷:77引用:2难度:0.1 -
2.已知在1200℃时,天然气脱硫工艺中会发生下列反应:
①H2S(g)+O2(g)═SO2(g)+H2O(g) ΔH132
②2H2S(g)+SO2(g)═S2(g)+2H2O(g) ΔH232
③H2S(g)+O2(g)═S(g)+H2O(g) ΔH312
④2S(g)═S2(g) ΔH4
则ΔH4的正确表达式为( )发布:2024/12/6 13:30:1组卷:400引用:6难度:0.5 -
3.氨和联氨(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用.联氨(又称肼,N2H4或H2N-NH2,无色液体)是一种应用广泛的化工原料,可用作火箭燃料.回答下列问题:
(1)联氨分子的电子式为,其中氮的化合价为;
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,该反应中还原剂与氧化剂的物质的量之比为2:1,反应的化学方程式为.
(3)①2O2(g)+N2(g)═N2O4(g)△H1
②ON2(g)+2H2(g)═N2H4(l)△H2
③O2(g)+2H2(g)═2H2O(g)△H3
④N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=-1038.6kJ•mol-1
上述反应热效应之间的关系式为△H4=,联氨和N2O4可作为火箭推进剂的主要原因为.
(4)联氨可用作火箭燃料,燃烧时发生的反应是N2O4(l)+2N2O4(l)═3N2(g)+4H2O(g)△H=-1038.6kJ•mol-1,若该反应中有4molN-H键断裂,则反应放出的热量为kJ.发布:2024/11/18 8:0:1组卷:12引用:0难度:0.9


