2023年人教新版中考化学复习专题:实验与探究题
发布:2024/9/20 15:0:11
一、选择题
-
1.操作规范是实验成功的关键。下列实验操作不正确的是( )
组卷:2引用:1难度:0.7 -
2.稀释浓硫酸并进行硫酸性质实验的操作中,正确的是( )
组卷:67引用:4难度:0.7 -
3.下列实验记录的数据或事故处理的方法,正确的是( )
组卷:2引用:1难度:0.5 -
4.下列有关家庭小实验说法错误的是( )
组卷:42引用:2难度:0.6
二、实验题
-
13.学习了常见的酸、碱后,同学们对碱的化学性质进行整理归纳,并在教师的指导下进行如下实验活动。
【验证实验】
【发现问题】通过实验,同学们发现实验三、实验四无明显现象,无法确定是否发生了化学反应,于是继续进行探究。序号 实验一 实验二 实验三 实验四 实验内容 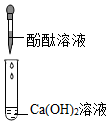
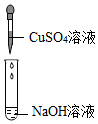
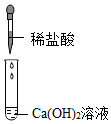
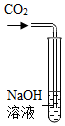
实验现象 溶液变 色产生蓝色沉淀 无明显现象 无明显现象 分析与结论 Ca(OH)2能与指示剂作用 反应的化学方程式为 无法确定是否发生反应 无法确定是否发生反应
【探究实验】
Ⅰ.取少量实验三中的剩余溶液,滴加溶液,溶液仍为无色,证明稀盐酸和Ca(OH)2溶液发生了化学反应,判断依据是溶液中完全反应了。
Ⅱ.取少量实验四中的剩余溶液,滴加溶液,观察到产生气体,证明CO2和NaOH溶液发生了化学反应。请写出产生气体的反应的化学方程式。
【总结提升】没有明显现象的化学反应,可以依据:A.检验反应物消失(或减少)或B.证明新物质生成这两种思路,利用间接观察法证明反应发生。上述两个实验设计实验方案的思路依据是:I;Ⅱ(填“A”或“B”)。组卷:34引用:1难度:0.5
三、科学探究题
-
14.碳酸氢钠是一种应用广泛的盐,化学小组对其进行了探究。
(1)NaHCO3可称为钠盐或碳酸氢盐,它是由Na+和(填离子符号)构成,医疗上能用于治疗胃酸(含有盐酸)过多症,反应的化学方程式为。
【提出问题】实验室中如何制取少量NaHCO3?
【查阅资料】
材料一:侯氏制碱的原理:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;2NaHCO3Na2CO3+CO2↑+H2O。△
材料二:研究发现,NaHCO3溶于水时吸收热量,Na2CO3溶于水时放出热量。
【实验制备】根据侯氏制碱原理设计如图1所示装置制取NaHCO3。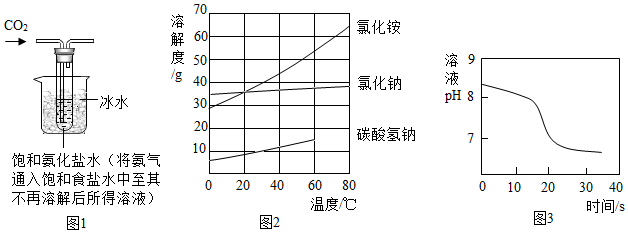
反应结束后,将试管中的混合物过滤洗涤,低温烘干得白色固体。
(2)烧杯中冰水的作用是。
(3)能进一步确认该白色固体是NaHCO3的实验方案是(须用到的仪器和药品:试管、温度计、水)。
(4)如图2中碳酸氢钠的溶解度在60℃后无数据的原因可能是。
【性质探究】
常温下,取一定量的NaHCO3溶液于烧杯中,插入pH传感器,向烧杯中持续滴加CaCl2溶液,有白色沉淀生成,当溶液的pH变为6.68时开始有无色气体产生。反应过程中溶液的pH随时间变化如图3所示。
【查阅资料】
材料三NaHCO3溶于水后,少量的能同时发生如下变化:HCO-3
变化①:+H2O→H2CO3+OH-;HCO-3
变化②:→HCO-3+H+。CO2-3
材料四:溶液的酸碱性与溶液中H+和OH-数目的相对大小有关。常温下,当单位体积溶液中OH-的数目大于H+的数目时溶液的pH>7,反之pH<7;单位体积溶液中所含的H+数目越大,溶液的pH越小。
【交流反思】
(5)NaHCO3溶液显(填“酸”“碱”或“中”)性,结合材料三、四从微观角度说明原因:。
(6)根据本实验,下列说法错误的是(填字母)。
a.pH<6.68时生成的无色气体为CO2
b.从0~30s,单位体积溶液中H+数目不断增大
c.不能用CaCl2溶液鉴别Na2CO3和NaHCO3溶液组卷:589引用:4难度:0.5


