2022-2023学年辽宁省部分重点中学高二(上)期末化学试卷
发布:2024/8/16 0:0:1
一、单项选择题(本题共15小题,每小题3分,共45分。每小题只有一个选项符合要求)
-
1.下列叙述正确的是( )
组卷:48引用:3难度:0.7 -
2.下列有关电解原理的应用的说法正确的是( )
组卷:53引用:3难度:0.5 -
3.短周期元素X、Y、Z原子序数依次增大,X元素基态原子有2个未成对电子,Y元素基态原子的核外p电子数比s电子数少1个,Z的一种“超原子”(
)具有40个价电子,下列说法错误的是( )Z-13组卷:43引用:3难度:0.7 -
4.①NH4HSO4②CH3COONH4③NH4HCO3④NH3⋅H2O四种溶液均为0.1mol/L,则下列关系正确的是( )
组卷:204引用:3难度:0.6 -
5.如图所示为锌铜原电池。下列叙述中正确的是( )
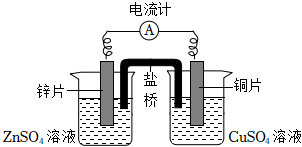 组卷:149引用:3难度:0.8
组卷:149引用:3难度:0.8 -
6.下列关于NH4+、NH3、NH2-三种微粒的说法不正确的是( )
组卷:522引用:15难度:0.5
二、填空题
-
18.处理、回收利用CO是环境科学研究的热点课题。回答下列问题:
(1)CO用于处理大气污染物N2O的反应为CO(g)+N2O(g)⇌CO2(g)+N2(g)。在Zn*作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。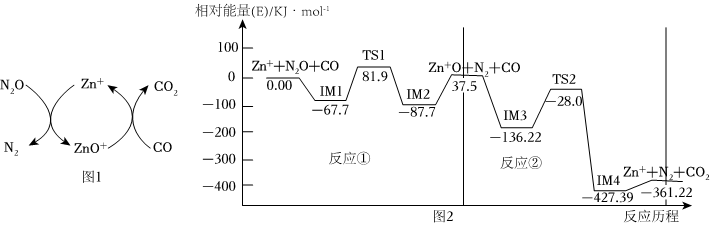
总反应:CO(g)+N2O(g)⇌CO2(g)+N2(g)ΔH=kJ⋅mol-1;该总反应的决速步是反应(填“①”或“②”),该判断的理由是。
(2)已知:CO(g)+N2O(g)⇌CO2(g)+N2(g)的速率方程为v=k⋅c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是(填字母序号)。
A.升温
B.恒容时,再充入CO
C.恒压时,再充入N2O
D.恒压时,再充入N2
(3)在总压为100kPa的恒容密闭容器中,充入一定量的CO(g)和N2O(g)发生上述反应,在不同条件下达到平衡时,在T1K时N2O的转化率与的变化曲线以及在n(N2O)n(CO)=1时N2O的转化率与n(N2O)n(CO)的变化曲线如图3所示:1T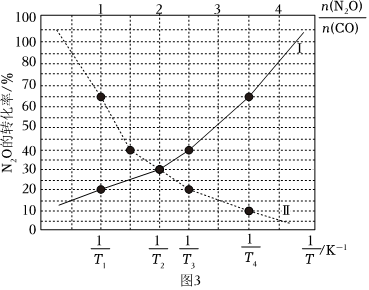
①表示N2O的转化率随的变化曲线为n(N2O)n(CO)曲线(填“Ⅰ”或“Ⅱ”);
②T1T2(填“>”或“<”);
③已知:该反应的标准平衡常数Kθ=,其中pθ为标准压强(100kPa),p(CO2)、p(N2)、p(N2O)和p(CO)为各组分的平衡分压,则T4时,该反应的标准平衡常数Kθ=p(CO2)pθ×p(N2)pθp(CO)pθ×p(N2O)pθ(计算结果保留两位有效数字,p分=p总×物质的量分数)。组卷:95引用:3难度:0.5 -
19.现有A、B、C、D、E、F、G7种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)C2A4的电子式为A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 B元素是形成化合物种类最多的元素 C元素的气态氢化物与其最高价氧化物的水化物可以成盐 D元素基态原子的核外p能级的原子轨道中有两个未成对电子 E元素的气态基态原子的第一至第四电离能分别是I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11575kJ/mol F元素的主族序数与周期数的差为4 G元素位于元素周期表中的第8列 (A、C为字母代号,请将字母代号用元素符号表示,下同)。
(2)B元素的原子核外共有种不同运动状态的电子,有种不同能量状态的电子。
(3)某同学推断E元素基态原子的核外电子轨道表示式为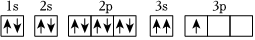 该同学所画的电子轨道表示式违背了 ,该元素的I4远远大于I3,其原因是。
该同学所画的电子轨道表示式违背了 ,该元素的I4远远大于I3,其原因是。
(4)D、E、F三种元素的简单离子半径由大到小的顺序是。
(5)G位于元素周期表中区(按电子排布分区)。组卷:69引用:2难度:0.5


