人教版(2019)选择性必修1《1.2.1 盖斯定律》2023年同步练习卷(4)
发布:2024/8/16 20:0:2
一、选择题
-
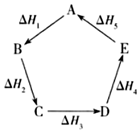 1.已知化学反应的热效应只与反应物的初始状态和生成物的最终状态有关,下列各反应热的关系不正确的是( )组卷:10引用:2难度:0.5
1.已知化学反应的热效应只与反应物的初始状态和生成物的最终状态有关,下列各反应热的关系不正确的是( )组卷:10引用:2难度:0.5 -
2.S(单斜)和S(正交)是硫的两种同素异形体.
已知:①S(单斜,s)+O2(g)═SO2(g)△H1=-297.16kJ•mol-1
②S(正交,s)+O2(g)═SO2(g)△H2=-296.83kJ•mol-1
③S(单斜,s)═S(正交,s)△H3
下列说法正确的是( )组卷:71引用:41难度:0.7 -
3.Mn2+催化H2O2分解:2H2O2(aq)═2H2O(l)+O2(g)△H1,其反应机理如下:
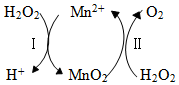
若反应Ⅱ的焓变为△H2,反应Ⅰ、Ⅱ的化学计量数均为最简整数比,则反应Ⅰ的焓变△H为( )组卷:235引用:11难度:0.5 -
4.N2O和CO是环境污染性气体,可在Pt2O+表面转化为无害气体,其反应为N2O(g)+CO(g)═CO2(g)+N2(g)△H,有关化学反应的物质变化过程如图1,能量变化过程如图2。下列说法正确的是( )
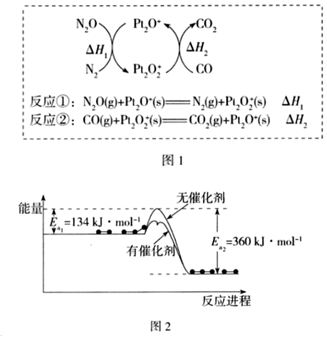 组卷:3引用:2难度:0.5
组卷:3引用:2难度:0.5 -
5.让生态环境更秀美、人民生活更幸福!为此,冬季取暖许多家庭用上了清洁能源天然气。实际生产中天然气需要脱硫,在1200℃时,工艺中会发生下列反应:①H2S(g)+
O2(g)═SO2(g)+H2O(g)△H1②2H2S(g)+SO2(g)═32S2(g)+2H2O(g)△H2③H2S(g)+32O2(g)═S(g)+H2O(g)△H3④2S(g)═S2(g)△H4则△H4的正确表达式为( )12组卷:224引用:4难度:0.5
三、解答题
-
15.尿素[CO(NH2)2]是首个由无机物人工合成的有机物.工业上合成尿素的反应为:2NH3(g)+CO2(g)⇌CO(NH2)2(l)+H2O(l)ΔH<0.回答下列问题:
(1)已知工业上合成尿素分两步进行,相关反应如下:
反应Ⅰ:2NH3(g)+CO2(g)⇌NH2COONH4(s)ΔH1<0
反应Ⅱ.NH2COONH4(s)⇌CO(NH2)2(l)+H2O(l)ΔH2>0;
下列示意图中[a表示2NH3(g)+CO2(g),b表示NH2COONH4(s),c表示CO(NH2)2(l)+H2O(l)],能正确表示尿素合成过程中能量变化的曲线是.
A.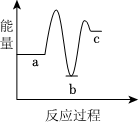
B.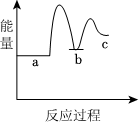
C.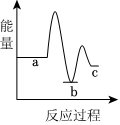
D.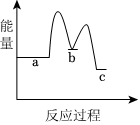
(2)在恒温恒容的密闭容器中充入物质的量之比为2:1的氨气和二氧化碳,发生反应:2NH3(g)+CO2(g)⇌CO(NH2)2(l)+H2O(l),可判断其达到平衡状态的是.
A.氨气的体积分数不再变化
B.氨气的转化率不再变化
C.气体的平均摩尔质量不再变化
D.气体的密度不再变化
(3)某实验小组甲模拟工业上合成尿素的条件,在恒定温度下,将氨气和二氧化碳按物质的量之比2:1充入一体积为10L的密闭容器中(假设容器体积不变,生成物的体积忽略不计),经20min达到平衡,各物质浓度的变化曲线如图所示.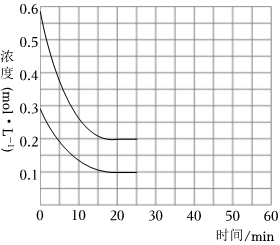
①在上述条件下,从反应开始至20min时,二氧化碳的平均反应速率为;
②实验小组乙为提高尿素的平衡产率,对甲组实验进行了改进(其它条件相同,且保持反应过程恒温恒容),下列可以采取的措施有;
A.改用5L的密闭容器
B.采用更高的温度
C.充入一定量的氦气
D.使用合适的催化剂
(4)甲组实验达到平衡后,25min时进行如下操作,请回答下列问题:
①若保持温度和容器容积不变,再充入2mol氨气和1mol二氧化碳,在40min时重新达到平衡,请在图中画出25~50min内氨气的浓度变化曲线.
②若保持温度和容器内气体压强不变,再充入3mol氨气,则此时v正v逆(填“>”“<”“=”),理由是.组卷:17引用:2难度:0.6 -
16.碳及其化合物有广泛的用途.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)═CO(g)+H2(g)△H>0,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2O(g)的平衡转化率的是.
A.升高温度 B.增加碳的用量 C.加入催化剂 D.用CO吸收剂除去CO
(2)将一定量的CO(g)和H2O(g)分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:
CO(g)+H2O(g)═CO2(g)+H2(g),得到如下数据:
通过计算求出该反应的平衡常数(计算结果保留两位有效数字).温度/℃ 起始量/mol 平衡量/mol 达到平衡所
需时间/minH2O CO
H2CO 900 1.0 2.0 0.4 1.6 3.0
(3)把水煤气中的混合气体经过处理后获得的较纯H2用于工业合成氨.已知:
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1
2N2(g)+6H2O(l)═4NH3(g)+3O2(g)△H=+1530.0kJ/mol
①氢气的燃烧热△H=.组卷:3引用:2难度:0.3


