人教版(2019)选择性必修1《专题2 化学反应速率与化学平衡(2)》2023年同步练习卷(1)
发布:2024/8/16 11:0:4
一、选择题
-
1.一定条件下,反应4NH3(g)+5O2(g)═4NO(g)+6H2O(g)在5L密闭容器中进行,10s时,水蒸气的物质的量增加了0.60mol,则前10s的平均反应速率为( )
组卷:88引用:6难度:0.9 -
2.一定条件下,将3mol A和1mol B两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(s)。2min末该反应达到平衡,生成0.8mol D,并测得C的浓度为0.4mol/L.下列判断正确的是( )
组卷:9引用:2难度:0.5 -
 3.一定温度下,向密闭容器中加入1.0molX,发生反应:2X(g)⇌Y(g)+Z(g)ΔH=-250kJ•mol-1,在14min时升高温度,X的物质的量浓度变化如图所示,下列说法正确的是( )组卷:4引用:3难度:0.6
3.一定温度下,向密闭容器中加入1.0molX,发生反应:2X(g)⇌Y(g)+Z(g)ΔH=-250kJ•mol-1,在14min时升高温度,X的物质的量浓度变化如图所示,下列说法正确的是( )组卷:4引用:3难度:0.6 -
4.2molA与2molB混合于2L的密闭容器中,发生如下反应:2A(g)+3B(g)⇌2C(g)+zD(g),若2s后,A的转化率为50%,测得v(D)=0.25mol/(L•s),下列推断正确的是( )
组卷:25引用:3难度:0.5
三、解答题
-
 17.过氧化氢(H2O2)是重要的化工产品,广泛应用于绿色化学合成、医疗消毒等领域。
17.过氧化氢(H2O2)是重要的化工产品,广泛应用于绿色化学合成、医疗消毒等领域。
回答下列问题:
(1)已知:H2(g)+O2(g)=H2O(l)△H1=-286kJ•mol-112
H2(g)+O2(g)=H2O2(l)△H2=-188kJ•mol-1
过氧化氢分解反应2H2O2(l)=2H2O(l)+O2(g)的△H=kJ•mol-1。
不同温度下过氧化氢分解反应的平衡常数K(313K)K(298K) (填>、<或=)。
(2)100℃时,在不同金属离子存在下,纯过氧化氢24h的分解率见下表:
由上表数据可知,能使过氧化氢分解反应活化能降低最多的离子是离子 加入量(mg•L-1) 分解率% 离子 加入量(mg•L-1) 分解率% 无 0 2 Fe3+ 1.0 15 Al3+ 10 2 Cu2+ 0.1 86 Zn2+ 10 10 Cr3+ 0.1 96 。
贮运过氧化氢时,可选用的容器材质为(填标号)。
A.不锈钢B.纯铝C.黄铜D.铸铁
(3)过氧化氢的Ka1=2.24×10-12,H2O2的酸性H2O (填>、<或=)。
研究表明,过氧化氢溶液中HO2-的浓度越大,过氧化氢的分解速率越快。常温下,不同浓度的过氧化氢分解率与pH的关系如图所示。一定浓度的过氧化氢,pH增大分解率增大的原因是:相同pH下,过氧化氢浓度越大分解率越低的原因是。组卷:745引用:6难度:0.5 -
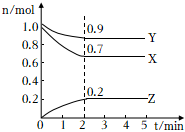 18.某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示,根据图中数据填空:
18.某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示,根据图中数据填空:
(1)该反应的化学方程式为。
(2)反应开始至2min,以气体Z表示的平均反应速率为。
(3)平衡时容器内混合气体密度与起始时相比,混合气体的平均相对分子质量与起始时相比。(填“变大”、“变小”或“不变”)
(4)amol X与bmol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足n(X)=n(Y)=2n(Z),则原混合气体中a:b=。组卷:2引用:2难度:0.5


