2024年江苏省盐城市建湖县中考化学二模试卷
发布:2025/11/7 16:0:43
一、选择题:本大题共15小题,每小题只有一个正确选项,每小题2分,共30分。
-
1.下列图示与相应的文字描述完全符合的是( )
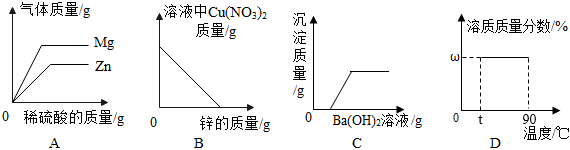 组卷:214引用:3难度:0.5
组卷:214引用:3难度:0.5 -
2.对乙酰氨基酚(C8H9NO2)是一种退烧止痛药,下列有关它的说法正确的是( )
组卷:46引用:3难度:0.9 -
3.原子是构成物质的基本粒子。下列有关原子的叙述错误的是( )
组卷:69引用:1难度:0.7 -
4.下列关于灭火的叙述中错误的是( )
组卷:39引用:2难度:0.5 -
5.建立模型是学习化学的重要方法,相关模型正确的是( )
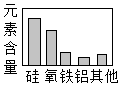

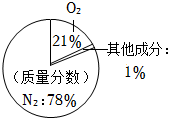
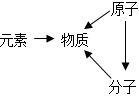
A.地壳中元素的含量 B.物质的分类 C.空气的组成 D.物质的组成和构成 组卷:73引用:5难度:0.5 -
6.下列实验中,能达到相应实验目的是( )
选项 实验目的 实验操作 A 鉴别(NH4)2SO4和K2SO4 取样,加入氯化钡溶液 B 分离碳酸钙和氯化钙的固体混合物 将混合物放入烧杯,加入足量水搅拌,充分溶解,过滤 C 制备氢氧化亚铁 向盛有一定量硫酸铁溶液的烧杯中,逐滴加入氢氧化钾溶液至过量,过滤 D 验证锌、铁,铜的金属活动性顺序 将形状完全相同的锌丝、铁丝、铜丝分别插入等量、等浓度的稀盐酸中 组卷:8引用:2难度:0.5 -
7.区分下列各组物质,选择的方法或试剂不正确的是( )
组卷:23引用:9难度:0.5 -
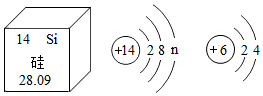 8.芯片是电脑、手机等的核心部件,碳基芯片采用石墨烯碳纳米管工艺,性能比硅基芯片更好,我国已突破半导体碳纳米管关键材料的技术瓶颈。如图是硅元素在元素周期表中的部分信息、原子结构示意图和碳原子结构示意图,下列有关说法错误的是( )组卷:28引用:2难度:0.5
8.芯片是电脑、手机等的核心部件,碳基芯片采用石墨烯碳纳米管工艺,性能比硅基芯片更好,我国已突破半导体碳纳米管关键材料的技术瓶颈。如图是硅元素在元素周期表中的部分信息、原子结构示意图和碳原子结构示意图,下列有关说法错误的是( )组卷:28引用:2难度:0.5 -
9.下列有关说法正确的是( )
组卷:10引用:1难度:0.5 -
10.在化学反应2A+B=C+2D中,12gA和10gB恰好完全反应生成8gC,则生成D的质量为( )
组卷:37引用:5难度:0.9 -
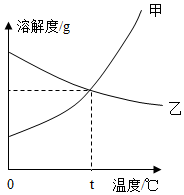 11.如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )组卷:29引用:2难度:0.4
11.如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )组卷:29引用:2难度:0.4 -
12.坚持绿色可持续发展已成为人们的共识,实施化肥农药减量增效行动有利于保护生态环境。下列属于复合肥料的是( )
组卷:223引用:5难度:0.8 -
13.6月5日为世界环境日。下列做法不利于保护环境的是( )
组卷:45引用:1难度:0.8 -
14.某同学要配制50g质量分数为14%的氯化钠溶液,下列关于配制该溶液的说法不正确的是( )
①若用氯化钠固体配制,需称取氯化钠固体7.0g
②选用200ml量筒量取所需水的体积
③实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和试剂瓶
④用量筒量取水时,俯视读数,配得溶液的溶质质量分数偏小.组卷:195引用:5难度:0.7 -
15.下列说法中,不正确的是( )
组卷:88引用:2难度:0.7
二、非选择题:本大题共4小题,共40分。
-
16.【关注生活现象】
“华夏古文明,山西好风光”。山西拥有丰富的非物质文化遗产,下面列举了其中的一部分,请运用所学知识,完成第11~14题。
世界面食在中国,中国面食在山西。面食为人体提供的营养素主要是,莜面是山西特产,其中含有对人体新陈代谢具有明显功效的物质-亚油酸(C18H32O2),从物质组成或构成的角度分析,由亚油酸的化学式可获得的一条信息是。组卷:9引用:0难度:0.6 -
17.在学习复分解反应发生的条件后,同学们利用已学知识,对稀盐酸与四种化合物溶液之间能否发生反应作出判断,并进行如图的实验验证:

(1)实验③观察到的现象是,实验②中不能发生反应的原因是,实验④的化学方程式是。
【提出问题】如何证明没有明显实验现象的物质间发生了化学反应?
【实验方案】以实验①为例,向NaOH溶液中加入以下可选试剂进行实验:酚酞试液、石蕊试液、稀盐酸、氯化铵溶液、硝酸银溶液。
【实验过程】
(2)上表中,a处试剂是组号 实验思路 操作 实验现象 结论 1 证明NaOH消失 向NaOH溶液中滴加a,再
逐滴加入过量的稀盐酸溶液先变红色,最终
变为无色稀盐酸与氢氧化钠能发生反应 2 证明NaOH消失 向反应后的溶液中滴入适
量氯化铜溶液b 3 证明NaCl生成 向反应后的溶液中滴入适
量AgNO3溶液有白色沉淀 ,b处现象是。
(3)有同学认为组号3实验设计不正确,理由是。组卷:41引用:1难度:0.5 -
18.根据如图装置,结合所学化学知识回答下列问题.
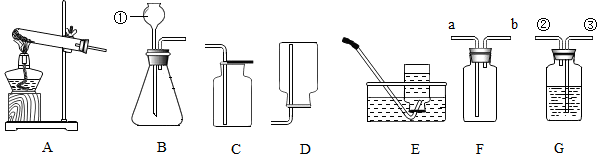
(1)请写标号仪器①的名称:;②
(2)实验室选择装置A用高锰酸钾制取氧气时,你认为A装置存在的问题是,可选用(填C或D)装置收集氧气.若用E装置收集氧气,收集满氧气后,应先,再熄灭酒精灯.该反应的化学方程式是.
(3)实验室用石灰石和稀盐酸制取CO2气体,该反应的化学方程式是验满的方法是;此法制得的二氧化碳,常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的G装置来除去,则混合气体应从G装置的端口(填“②”或“③”)通入,实验室用稀盐酸和石灰石制取CO2气体,而不用稀硫酸和石灰石,原因是.
(4)将CO2通入紫色石蕊溶液中,溶液变成红色,加热后溶液又变成紫色,用化学方程式表示加热后又变成紫色的原因:.
(5)通常情况下,SO2是一种无色、有刺激性气味的气体,密度比空气大,易溶于水且水溶液显酸性.实验室里,用亚硫酸钠固体和浓硫酸反应制取SO2.实验室制取SO2选择的发生装置是(填字母),若选择F装置收集SO2,气体应该从口(填“a”或“b”)进入,实验结束后剩余的SO2气体用氢氧化钠溶液吸收,吸收的目的是.组卷:33引用:3难度:0.5 -
19.【资料在线】①NaN3受撞击会生成Na、N2.
②NaN3遇盐酸、H2SO4溶液无气体生成.
③碱石灰是CaO和 NaOH的混合物.④NaN3与可溶性的钙盐、钡盐不反应.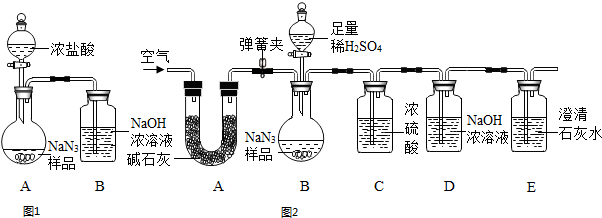
【问题探究】
(1)NaN3的制备方法是:将金属钠与液态氨反应制得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和气体X,该反应的化学方程式为2NaNH2+N2O=NaN3+NaOH+X;则X的化学式为,实验室检验X气体的方法是.
(2)工业级NaN3中常含有少量的Na2CO3,其原因是(用化学方程式表示).
【Na2CO3纯度测定】
(3)为测定某工业级NaN3样品中含有Na2CO3的质量分数,化学小组同学设计了如图实验.
①小明同学认为通过测定如图1中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的纯度,小组内同学通过讨论认为不可以,其理由可能是.
②小刚同学在大家讨论的基础上,设计了装置如图2.请分析:图2中A的作用是;若无装置C,对测定结果造成的影响是(填“偏大”、“偏小”或“无影响”);装置E的作用是.
③小静同学认为取少量NaN3样品溶于水,滴加过量的Ba(NO3)2溶液也可以测定Na2CO3的质量分数,则如何判断滴加的试剂已过量.
【NaN3纯度测定】
精确称量0.140g NaN3样品,设计如图3装置测定其纯度.已知2NaN3→3N2(NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热.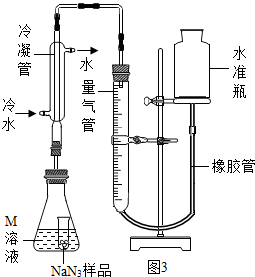
(4)使小试管中的NaN3样品与M溶液接触的操作是:.
(5)使用冷水冷凝的目的是:.反应前应将液面调节到量气管的“0”刻度,并使两边液面相平,反应后读数时,还需要进行的操作是.
(6)常温下测得量气管读数为67.2mL(N2的密度为1.25g/L),则实验中选用的量气管规格合适的是(填字母序号).
A.100mL B.1L C.2L
(7)计算NaN3样品的纯度.(精确到0.1%)组卷:38引用:2难度:0.1


