2022-2023学年重庆市高一(下)期末化学试卷
发布:2024/6/27 8:0:9
一、选择题(每题只有一个选项符合题意,每题3分,共48分)
-
1.下列设备工作时,将化学能转化为电能的是( )
A B C D 



锂离子电池 硅太阳能电池 电动车电池充电 燃气灶 组卷:35引用:4难度:0.7 -
2.化学与生活、社会发展息息相关,下列说法错误的是( )
组卷:8引用:2难度:0.7 -
3.下列化学用语正确的是( )
组卷:9引用:2难度:0.7 -
4.资源、能源、环保、安全等是当今社会重要的议题。下列有关说法不正确的是( )
组卷:17引用:2难度:0.7 -
5.根据下列实验事实得出的相应结论正确的是( )
实验事实 结论 A NH3的水溶液可以导电 NH3是电解质 B 浓硫酸能使蓝色胆矾晶体变成白色 浓硫酸具有强氧化性 C 加入浓NaOH溶液,并加热.试管口附近,湿润的红色石蕊试纸变蓝 原溶液中含有 NH+4D SO2通入硝酸钡溶液出现白色沉淀 BaSO3不溶于强酸 组卷:9引用:2难度:0.5 -
6.如图所示,有关化学反应和能量变化的说法正确的是( )
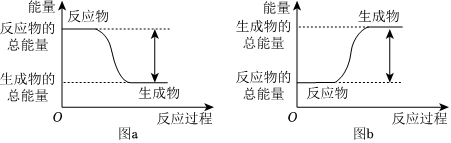 组卷:132引用:2难度:0.7
组卷:132引用:2难度:0.7
第Ⅱ卷(非选择题,共52分)
-
19.从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。如图是硫、氮两元素的价类二维图.请回答下列问题:
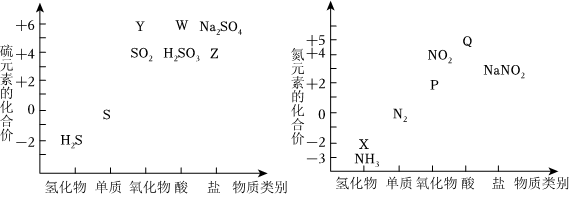
(1)物质Y是H2SO4的酸酐,其分子式为。
(2)大苏打(Na2S2O3)在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途.现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是。(填字母)
A.Na2S+S
B.Na2SO3+S
C.Na2SO3+Na2SO4
D.Na2SO3+H2SO4
(3)W的浓溶液具有强氧化性、吸水性和脱水性,常用作干燥剂,则下列气体可用W干燥的是。(填字母)
A.SO2
B.H2S
C.NH3
D.HI
(4)在化工生产中,需要考虑控制反应条件.工业合成氨通常选择在10MPa~30MPa下进行,压强不能过低也不能过高的原因是:。
(5)已知物质Z是一种可溶性正盐,能被酸性K2Cr2O7溶液氧化为Na2SO4,Cr2被还原为Cr3+,请写出此反应的离子方程式O2-7。
(6)将32g铜与150mL一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质P和二氧化氮混合气体共11.2L.待产生的气体全部释放后,向溶液加入200mL5mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则物质Q的物质的量浓度是mol/L。组卷:29引用:2难度:0.5 -
20.工业废气在排放前需进行预处理,以达到国家废气对外排放的标准。煤燃烧产生的烟气也属于工业废气,含有 SO2和NOx石油化工生产过程中产生H2S需采用有效措施对烟气和生产过程进行脱硫、脱硝,减少对大气的污染。
Ⅰ.脱H2S
(1)Fe2(SO4)3溶液脱除烟气中H2S 并再生的原理如图所示。Fe2(SO4)3的作用是。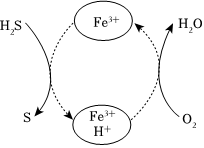
Ⅱ.脱SO2和NOx
(2)一种处理含的废水和工业废气(主要含 N2、CO2、SO2、NO、CO)的流程如图:NH+4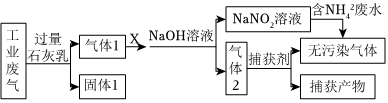
已知:用NaOH溶液吸收NOx,反应原理为:2NO2+2NaOH=NaNO2+NaNO3+H2O;NO+NO2+2NaOH=2NaNO2+H2O;
①固体1的主要成分有Ca(OH)2、、。
②X为氧气,其作用是(用化学方程式表示)。
③处理含废水时,发生反应的离子方程式为NH+4。
(3)工业废气中的CO和NO,还可以发生如下反应:2CO(g)+2NO(g)⇌2CO2(g)+N2(g)。在恒温恒容的密闭容器中,充入等物质的量的CO和NO混合气体,发生上述反应,t0时达到平衡,测得反应过程中CO2 的体积分数与时间的关系如图所示。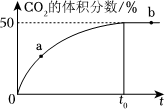
①比较大小:a处v正b处v逆 (填“>”、“<”或“=”)。
②平衡后往该密闭容器中再充入一定量的氦气,则CO2的体积分数50%。(填“>”、“<”或“=”)
③能说明上述反应已达化学平衡状态的是(填字母)。
A.v正(CO)=v逆(NO)
B.混合气体密度保持不变
C.反应容器内压强保持不变
D.断开2mol C=O键同时生成1mol N≡N键组卷:24引用:2难度:0.7


