2023-2024学年北京交大附中高二(上)期中化学练习试卷
发布:2024/10/2 5:0:2
一、选择题(每小题只有一个选项符合题意,本题共14小题,每小题3分,共42分)
-
1.下列装置或过程能实现电能转化为化学能的是( )

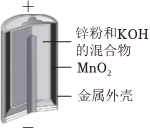
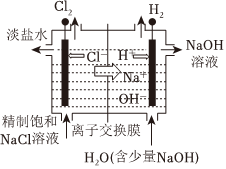
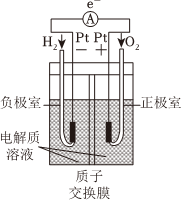
A.火力发电 B.碱性锌锰电池 C.电解饱和食盐水 D.氢氧燃料电池 组卷:37引用:3难度:0.7 -
2.下列说法正确的是( )
组卷:313引用:13难度:0.8 -
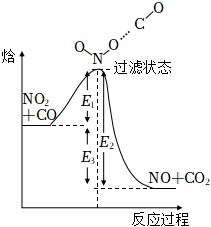 3.如图所示为某基元反应过程的能量变化(E1、E2、E3均大于0)。下列说法正确的是( )组卷:84引用:7难度:0.7
3.如图所示为某基元反应过程的能量变化(E1、E2、E3均大于0)。下列说法正确的是( )组卷:84引用:7难度:0.7 -
4.一定温度下,在2个容积均为10L的恒容密闭容器中,加入一定量的反应物,发生反应:H2(g)+I2(g)⇌2HI(g),充分反应并达到化学平衡状态,相关数据见下表。下列说法正确的是( )
容器编号 起始时各物质的物质的量/mol 平衡时I2的浓度/(mol•L-1) n(H2) n(I2) n(HI) c(I2) Ⅰ 0.1 0.1 0 0.008 Ⅱ 0.2 0.2 0 x 组卷:76引用:7难度:0.4 -
5.化学小组研究金属的电化学腐蚀,实验如下:
下列说法不正确的是( )序号 实验Ⅰ 实验Ⅱ 实验 

现象 铁钉周边出现______色
锌片周边未见明显变化铁钉周边出现蓝色
铜片周边略显红色组卷:211引用:6难度:0.5 -
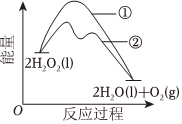 6.已知1molH2O2分解放出热量98kJ。在含有少量I-的溶液中,H2O2分解的机理是:ⅰ.H2O2+I-═H2O+IO-,ⅱ.H2O2+IO-═H2O+O2↑+I-。H2O2分解过程中能量变化如图。下列说法正确的是( )组卷:87引用:5难度:0.5
6.已知1molH2O2分解放出热量98kJ。在含有少量I-的溶液中,H2O2分解的机理是:ⅰ.H2O2+I-═H2O+IO-,ⅱ.H2O2+IO-═H2O+O2↑+I-。H2O2分解过程中能量变化如图。下列说法正确的是( )组卷:87引用:5难度:0.5
二、第Ⅱ卷(58分)
-
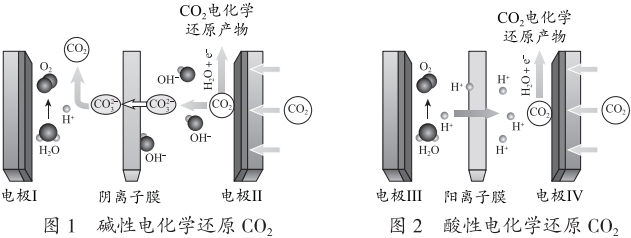
18.电化学还原CO2将其转化为其它化学产品,是一种综合利用CO2的好方法。
已知:选择性(S)和法拉第效率(FE)的定义:
S(B)=×100%n(生成B所用的CO2)阴极吸收的CO2
FE(B)=×100%n(生成B所用的电子)n(通过电极的电子)
(1)碱性电化学还原CO2前,先在中性电解液中通电一段时间,pH及电流稳定后,再通CO2。在阴极区若CO2每得到1mol电子,同时H2O也会得到等物质的量的电子,且阴极区电解液的pH几乎保持不变(忽略溶液体积变化)。
①补全阴极产生CH4的电极反应:CO2++═CH4+。
②阴极附近因为发生反应(用离子方程式表示),生成的难以放电,降低了S(CH4)。结合上述信息,S(CH4)的理论最大值为CO2-3。
③结合化学用语分析阳极区产生CO2的原因是。
(2)控制pH=1、电解液中存在KCl时,电化学还原CO2过程中CH4(其他含碳产物未标出)和H2的法拉第效率变化如图3所示。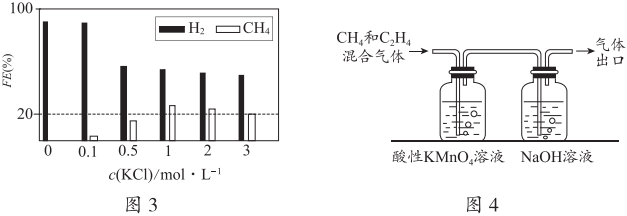
①结合图3的变化规律,推测KCl可能的作用是。
②c(KCl)=3mol•L-1时,11.2L(已折合为标准状况,下同)的CO2被完全吸收并还原为CH4和C2H4,分离H2后,将CH4和C2H4混合气体通入如图4所示装置(反应完全),出口处收集到气体6.72L,则FE(C2H4)为。组卷:103引用:4难度:0.5 -
19.实验小组对NaHSO3溶液分别与CuCl2、CuSO4溶液的反应进行探究。
已知:实验 装置 试剂x 操作及现象
Ⅰ
1 mol•L-1 CuCl2溶液加入2mL CuCl2溶液,得到绿色溶液,30s时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 Ⅱ 1 mol•L-1 CuSO4溶液 加入2mL CuSO4溶液,得到绿色溶液,3分钟未见明显变化。
Ⅰ.Cu2+[Cu(NH3)4]2+(深蓝色溶液)浓氨水
Ⅱ.Cu+[Cu(NH3)2]+(无色溶液)浓氨水[Cu(NH3)4]2+(深蓝色溶液)露置在空气中一段时间
(1)推测实验Ⅰ产生的无色气体为SO2,实验证实推测正确:用蘸有碘水的淀粉试纸接近试管口,观察到,反应的离子方程式为。
(2)对实验Ⅰ产生SO2的原因进行分析,提出假设:
假设a:Cu2+水解使溶液中c(H+)增大;
假设b:Cl-存在时,Cu2+与反应生成CuCl白色沉淀,溶液中c(H+)增大。HSO-3
①假设a不合理,实验证据是;
②实验表明假设b合理,实验I反应的离子方程式有、H++═SO2↑+H2O。HSO-3
(3)对比实验Ⅰ、Ⅱ,提出假设:Cl-增强了Cu2+的氧化性。
下述实验Ⅲ证实了假设合理,装置如图。实验方案:闭合K,电压表的指针偏转至“X”处;向U形管(补全实验操作及现象)。
(4)将实验Ⅱ的溶液静置24小时或加热后,得到红色沉淀。经检验,红色沉淀中含有Cu+、Cu2+和。SO2-3
①通过实验Ⅳ证实红色沉淀中含有Cu+和Cu2+。
实验Ⅳ: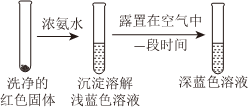
证实红色沉淀中含有Cu+的实验证据是;
②有同学认为实验Ⅳ不足以证实红色沉淀中含有Cu2+,设计实验Ⅳ的对比实验Ⅴ,证实了Cu2+的存在。实验Ⅴ的方案和现象是:。组卷:105引用:6难度:0.5


