人教版(2019)必修第一册《专题四 元素推断与周期律的应用》2023年同步练习卷
发布:2024/8/8 8:0:9
一、选择题
-
1.短周期元素A、B、C原子序数依大增大,A3-与B2-、C+电子层结构相同,则下列说法中不正确的是( )
组卷:25引用:5难度:0.6 -
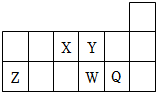 2.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )组卷:1480引用:104难度:0.5
2.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )组卷:1480引用:104难度:0.5 -
3.X、Y、Z、W为四种短周期主族元素,且原子序数依次增大.已知X的最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,Y原子的最外层电子数是W原子最外层电子数的2倍,Z原子最外层只有一个电子.下列说法正确的是( )
组卷:129引用:5难度:0.7 -
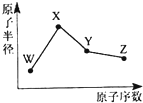 4.W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差l;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法不正确的是( )组卷:23引用:9难度:0.9
4.W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差l;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法不正确的是( )组卷:23引用:9难度:0.9
三、解答题
-
 11.短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素。
11.短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素。
请用化学用语回答下列问题:
(1)A、D、E元素简单离子半径由大到小的顺序为>>(填粒子符号)
(2)F与D同主族且相邻二者气态氢化物稳定性的大小关系为>(填粒子符号)
(3)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放出一个电子,同时产生一种
具有较强氧化性的阳离子,试写出该阳离子的电子式:。 该阳离子中存在的化学键有。
(4)由C、E两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子中C、E两种原子最外层均达到8个电子的稳定结构。甲遇水蒸气可形成一种常见的漂白性物质。写出甲遇水蒸气的化学方程式。组卷:6引用:2难度:0.5 -
12.甲图是部分短周期元素的常见化合价与原子序数的关系图。
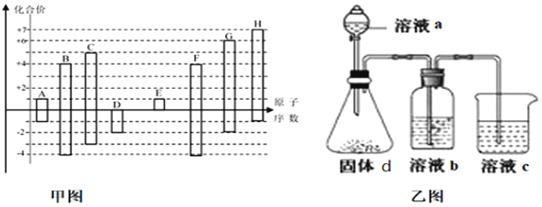
请回答下列问题:
(1)甲图中C元素的中子数为7,其原子符号为,元素I与G同主族,位于第四周期,则元素I的原子结构示意图。
(2)F、G、H元素气态氢化物的稳定性由强到弱的顺序为。(用化学式表示)
(3)化合物X是B元素的最高价氧化物,其电子式为,甲图中C元素的一种氢化物Y是10电子微粒,Y与O2发生置换反应的化学方程式为。
(4)H的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是H的单质,且当有28mol电子转移时,恢复至室温共产生9mol气体,写出该反应的化学方程式。
(5)由上述元素中的几种组成a、b、c、d各物质,某同学设计实验用乙图装置证明元素B、C、F的非金属性强弱(其中溶液b和溶液c均为足量)。
①溶液a和b分别为,。(填化学式)
②溶液c中的离子方程式为。
③请从原子结构的角度解释非金属性C>B的原因。组卷:9引用:2难度:0.5


