人教版(2019)选择性必修1《2.2.2 化学平衡常数 影响化学平衡的因素》2023年同步练习卷(7)
发布:2024/8/16 18:0:1
一、选择题
-
1.可以作为判断化学平衡发生移动的标志是( )
组卷:28引用:4难度:0.7 -
2.在水溶液中,CrO42-呈黄色,Cr2O72-呈橙红色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O72-+H2O⇌2CrO42-+2H+,下列说法正确的是( )
组卷:58引用:6难度:0.6 -
3.下列说法正确的是( )
组卷:58引用:3难度:0.5 -
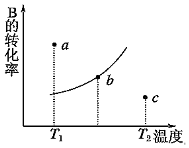 4.有一反应:2A(g)+B(g)⇌2C(g),如图中的曲线是该反应在不同温度下的平衡曲线,则下列描述不正确的是( )组卷:69引用:3难度:0.7
4.有一反应:2A(g)+B(g)⇌2C(g),如图中的曲线是该反应在不同温度下的平衡曲线,则下列描述不正确的是( )组卷:69引用:3难度:0.7 -
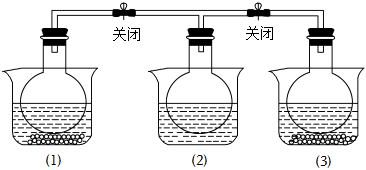 5.如图,在三个圆底烧瓶中都充满NO2气体,并分别放置在加有下列物质的烧杯(烧杯内有水)中:在(1)中加入CaO,(2)中不加其他任何物质,在(3)中加入NH4Cl晶体。发现:(1)中红棕色变深,(3)中红棕色变浅。下列叙述正确的是( )组卷:2引用:3难度:0.7
5.如图,在三个圆底烧瓶中都充满NO2气体,并分别放置在加有下列物质的烧杯(烧杯内有水)中:在(1)中加入CaO,(2)中不加其他任何物质,在(3)中加入NH4Cl晶体。发现:(1)中红棕色变深,(3)中红棕色变浅。下列叙述正确的是( )组卷:2引用:3难度:0.7 -
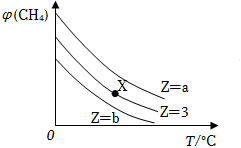 6.一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)⇌CO(g)+3H2(g)设起始=Z,在恒压下,平衡时φ (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是( )n(H2O)n(CH4)组卷:975引用:41难度:0.7
6.一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)⇌CO(g)+3H2(g)设起始=Z,在恒压下,平衡时φ (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是( )n(H2O)n(CH4)组卷:975引用:41难度:0.7
三、解答题
-
22.超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO
2CO2+N2.为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:催化剂
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):时间(s) 0 1 2 3 4 5 c(NO)
(mol/L)1.00×10-3 4.50×10-4 2.50×10-4 1.50×10-4 1.00×10-4 1.00×10-4 c(CO)
(mol/L)3.60×10-3 3.05×10-3 2.85×10-3 2.75×10-3 2.70×10-3 2.70×10-3
(1)在上述条件下反应能够自发进行,则反应的△H0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(NO)=。
(3)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是。
A.选用更有效的催化剂
B.升高反应体系的温度
C.降低反应体系的温度
D.缩小容器的体积
(4)在该温度下,反应的平衡常数K=。组卷:3引用:3难度:0.7 -
23.随着氮氧化物对环境及人类活动影响的日趋严重,如何消除大气污染物中氮氧化物成为人们关注的主要问题之一。
Ⅰ.利用NH3的还原性可以消除氮氧化物的污染。
(1)请写出NH3的电子式。
(2)已知:①H2O(l)═H2O(g)△H1=+44.0KJ•mol-1
②N2(g)+O2(g)═2NO(g)△H2=+229.3KJ•mol-1
③4NH3(g)+5O2(g)═4NO(g)+6H2O( g)△H3=-906.5 KJ•mol-1
则反应④4NH3(g)+6NO(g)═5N2(g)+6H2O(l) 的△H=;该反应的平衡常数K的表达式为;增加压强,该反应中NO的转化率将(填“提高”、“不变”或“降低”)。
(3)一定温度下,在容积固定的密闭容器中,发生反应④,下列能判断该反应达到平衡的是(填标号)
A.c(NH3)=c(N2) B.容器中压强不变
C.容器中混合气体的密度不变D.1molN-H键断裂的同时,生成1molO-H键
(4)某小组研究了NH3和NO在Ag2O催化剂表面发生上述反应④,其中NO在一定时间内的转化率随温度变化的结果如图1所示。在有氧条件下,温度580K之后NO生成N2的转化率降低的原因可能是。在温度为420~580K时,有氧条件下NO生成N2的转化率明显高于无氧条件的原因可能是。
Ⅱ.用尿素[(NH2)2CO]水溶液吸收氮氧化物也是一种可行的方法。NO和NO2不同配比混合气通入尿素溶液中,总氨还原率与配比关系如图2。
(5)用尿素[(NH2)2CO]水溶液吸收体积比为1:1的NO和NO2混合气,将N元素转变为对环境无害的气体写出该反应的化学方程式。
(6)随着NO和NO2配比的提高,总氮还原率降低的主要原因是。组卷:21引用:2难度:0.5


