2023-2024学年广东省东莞市东华高级中学高二(上)开学化学试卷
发布:2024/8/25 1:0:8
一、单选题(1-10题每题2分,11-16题每题4分,共44分)
-
1.糖类、油脂、蛋白质都是与生命息息相关的物质,下列有关说法正确的是( )
组卷:199引用:5难度:0.6 -
2.诺贝尔化学奖获得者艾哈迈德•泽维尔开创了“飞秒化学”的新领域,使运用激光技术、光谱技术观察化学反应时分子中原子的运动成为可能。据此,你认为该技术确定能观察到的是( )
组卷:4引用:4难度:0.7 -
3.关于化合物2-苯基丙烯(
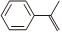 ),下列说法正确的是( )组卷:2302引用:44难度:0.7
),下列说法正确的是( )组卷:2302引用:44难度:0.7 -
4.下列实验或生产过程及其解释均正确且有对应关系的是( )
选项 实验或生产过程 解释 A FeCl3溶液蚀刻铜制印刷电路板 金属性:Fe>Cu B Cu和稀硝酸反应,在试管口有红棕色气体 Cu和稀硝酸反应生成NO2 C 新制的氯水长时间放置后,酸性增强 HClO易分解产生HCl D 工业上通过电解熔融MgO制取金属Mg MgO熔点低 组卷:29引用:3难度:0.5 -
5.已知反应:2H2O2═2H2O+O2↑,下列措施不能加快该反应的速率的是( )
组卷:62引用:2难度:0.7 -
6.将Al条插入6mol•L-1的盐酸中,反应过程中产生H2速率的变化情况如图1所示。下列说法错误的是( )
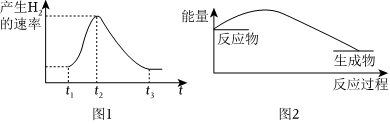 组卷:66引用:3难度:0.5
组卷:66引用:3难度:0.5
二、解答题(共56分)
-
19.工业合成氨反应为N2(g)+3H2(g)⇌2NH3(g),氨在工农业生产中应用广泛。
(1)已知:键能是1mol化学键完全断裂形成气态原子所需要吸收的能量,部分化学键的键能如表格所示。计算每合成2molNH3需要化学键 H-H N-H N≡N 键能(kJ•mol-1) 436 391 945.6 (填“放出”或“吸收”)kJ的热量。
(2)实验室中模拟合成氨过程,将1molN2和2.7molH2置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是(填序号)。
a.反应不再进行,已经停止
b.单位时间内生成nmolN2的同时,生成3nmolH2
c.3v正(H2)=2v逆(NH3)
d.N2、H2和NH3的物质的量浓度之比为1:3:2
e.混合气体的压强不再改变
f.混合气体的密度不再改变
若10min时测得氢气浓度为1.2mol•L-1,则用氨气表示的0~10min内的平均化学反应速率为;10min时的体系总压强与初始时的总压强之比为。
(3)工业合成氨过程中,按一定投料比将原料气以及催化剂置于反应容器中,测得在不同温度和压强下达到化学平衡状态时的氨的平衡含量(%)如表格所示:
实际生产时,通常采用铁触媒作为催化剂、在400~500℃和10~30MPa的条件下合成氨。结合所学知识以及上述表格数据分析,工业上采用400~500℃反应的原因是压强(MPa)
氨的平衡含量(%)
温度(摄氏度)0.1 10 20 30 60 100 200 15.3 81.5 86.4 89.9 95.4 98.8 300 2.2 52.0 64.2 71.0 84.2 92.6 400 0.4 25.1 38.2 47.0 65.2 79.8 500 0.1 10.6 19.1 26.4 42.2 57.5 600 0.05 4.5 9.1 13.8 23.1 31.4 。
(4)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池的工作原理如图所示。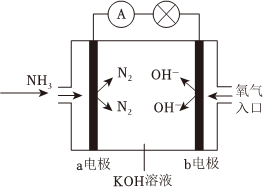
a电极的电极反应式是。
b电极的电极反应式是。组卷:9引用:1难度:0.7 -
20.丙烯是一种重要的化工原料,以丙烯为原料衍生出部分化工产品的反应如图(部分反应条件已略去)。请回答下列问题:
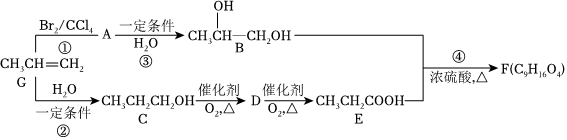
(1)A的结构简式为。
(2)反应①②③④中,属于加成反应的是(填序号)。
(3)有机物B、D中含有的官能团的名称分别为、。
(4)聚丙烯(英文缩写:PP)具有机械强度高、耐化学腐蚀等特性,可用于制作薄膜、管道等,写出聚丙烯的结构简式:。
(5)写出下列反应的化学方程式
①C→D:。
②B+E→F:。
(6)由B和E制取F的过程中,向制得的F的混合溶液中加入5%碳酸钠溶液充分混合,则碳酸钠的作用是。组卷:21引用:4难度:0.5


