人教版(2019)选择性必修1《1.1.1 反应热 焓变》2023年同步练习卷(1)
发布:2024/8/16 21:0:1
一、选择题
-
1.用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算反应热。下列关于实验和中和反应的说法正确的是( )
 组卷:94引用:5难度:0.7
组卷:94引用:5难度:0.7 -
2.在测定中和热的实验中,下列说法正确的是( )
组卷:214引用:7难度:0.9 -
3.下列说法正确的是( )
组卷:50引用:14难度:0.9 -
4.下列变化一定为放热的化学反应的是( )
组卷:78引用:7难度:0.9 -
5.下列说法不正确的是( )
组卷:7引用:2难度:0.9
二、填空题
-
14.下列说法正确的是
.
A.化学反应在物质变化的同时,伴随着能量变化,其表现形式只有吸热和放热两种
B.所有燃烧反应都是放热反应,所以不需吸收能量就可以进行
C.若一定条件下,A═B△H<0,说明A物质比B物质稳定
D.“冰,水为之,而寒于水”说明相同质量的水和冰相比较,冰的能量高
E.相同条件下,如果1mol氢原子所具有的能量为E1,1mol氢分子的能量为E2,则2E1>E2
F.测定盐酸和氢氧化钠反应的中和热实验中,所用试剂可以是浓溶液
G.1molNaOH分别和1molCH3COOH、1molHNO3反应放出的热量:CH3COOH<HNO3
H.HCl和NaOH反应的中和热△H=-57.3 kJ•mol-1,则1molH2SO4和1molBa(OH)2反应放出的热量为114.6kJ
I.对于可逆反应,反应进行的净速率是正、逆反应速率之差
J.把铝条放入盛有过量稀盐酸的试管中,加入Na2SO4溶液不影响氢气产生速率
K.已知C(s)与CO(g)的燃烧热(△H)分别为-393.5kJ•mol-1、-283.0kJ•mol-1,则相同条件下C(s)与O2(g)反应生成1molCO(g)的反应热为△H=-110.5kJ/mol
L.对于可逆反应,正、逆反应速率的比值是恒定的.组卷:21引用:2难度:0.5 -
15.(1)如图1是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,则E1
(填“增大”、“减小”或“不变”,下同),ΔH。请写出NO2和CO反应的热化学方程式:。
(2)观察图a和图b,根据盖斯定律,写出ΔH1、ΔH2、ΔH3、ΔH4、ΔH5和ΔH6的关系。图a:;图b:。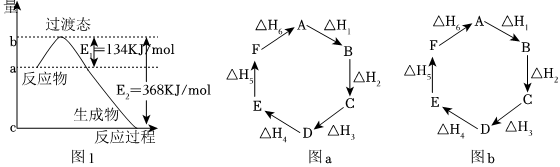
(3)用CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:①H2O(l)═H2O(g)ΔH=+44kJ/mol
②2N2(g)+CO2(g)+2H2O(g)═CH4(g)+4NO(g)ΔH=+1160kJ/mol
③CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ/mol
请写出CH4(g)与NO2(g)反应生成参与大气循环的气体和液态水的热化学方程式。组卷:29引用:3难度:0.7


