人教版(2019)选择性必修1《2.2.4 影响化学平衡的因素(二)》2023年同步练习卷(10)
发布:2024/8/16 18:0:1
一、选择题
-
1.在一密闭容器中,反应aA(g)⇌bB(g)达到平衡后,保持温度不变,将容器体积缩小一半,当达到新平衡时,B的浓度是原来的1.8倍,则( )
组卷:8引用:4难度:0.9 -
2.反应CO(g)+H2O(g)⇌CO2(g)+H2(g)在800℃达到平衡时,分别改变下列条件,K值会发生变化的是( )
组卷:28引用:2难度:0.9 -
3.在一密闭容器中,一定条件下,进行如下反应:2NO(g)+2CO(g)⇌N2(g)+2CO2(g);△H=-373.2kJ/mol,达到平衡后,为提高NO的转化率,采取的正确措施是( )
组卷:3引用:2难度:0.9
三、解答题
-
13.做好碳达峰、碳中和工作,是中央经济工作会议确定的2021年八项重点任务之一。CO2的资源化可以推动经济高质量发展和生态环境质量的持续改善。
(1)一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH1
反应2:CO(g)+2H2(g)⇌CH3OH(g)ΔH2
反应3:CO2(g)+3H2(g)⇌CH3OH(g)+H2O ΔH3
其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图1所示。则ΔH2ΔH3(填“大于”、“小于”或“等于”)。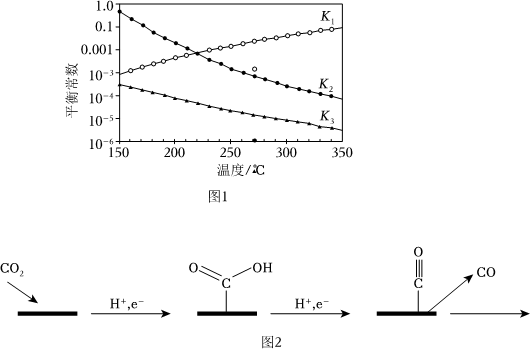
(2)对于上述CO2加氢合成CH3OH的体系,下列说法错误的是(填标号)。
A.增大H2浓度有利于提高CO2的转化率
B.当气体的平均相对分子质量保持不变时,说明反应体系已达平衡
C.体系达平衡后,若压缩体积,则反应1平衡不移动,反应3平衡正向移动
D.选用合适的催化剂可以提高CH3OH在单位时间内的产量。
已知对于反应:aA(g)+bB(g)⇌cC(g)+dD(g)其标准平衡常数:kΘ=,某温度为T,压强为16pΘ的恒压密闭容器中,通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol(b>a),此时H2O(g)的分压p(H2O)=[p(C)pΘ]c×[p(D)pΘ]d[p(A)pΘ]a[p(B)pΘ]b(用含a、b的代数式表示,下同),反应1的标准平衡常数为。
(3)电催化还原能将CO2转化为多种碳产物。在铜电极上将CO2还原为CO的机理如图2所示。写出该机理过程总的电极方程式:。
(4)利用CO2为原料可以合成苯乙烯,涉及以下反应:
Ⅰ、C6H5-C2H5(g)⇌C6H5-CH═CH2(g)+H2(g) Kp1=2.7×10-15 ΔHⅠ=23.47kJ•mol-1
Ⅱ、H2(g)+O2(g)═H2O(g) Kp2=1.26×1040 ΔHⅡ=-241.82kJ•mol-112
结合数据说明乙苯制苯乙烯过程中加氧气的理由。组卷:51引用:2难度:0.6 -
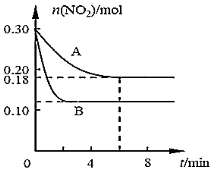 14.在A、B两个恒容密闭容器中发生反应:2NO2⇌2NO+O2反应过程中NO2的物质的量随时间变化的状况如图所示。
14.在A、B两个恒容密闭容器中发生反应:2NO2⇌2NO+O2反应过程中NO2的物质的量随时间变化的状况如图所示。
(1)若A容器的体积为5L,反应经6min达到平衡状态,则0~6min内以O2浓度变化表示的反应速率为。
(2)该反应化学平衡常数K=(写出表达式)。
(3)说明该反应已达到平衡状态的是。
A.v正(NO2)=v逆(NO) B.c(NO2)=c(NO)
C.气体的平均摩尔质量不变 D.气体的密度保持不变
(4)若A、B两容器中只是温度不同,则TATB (填“>”或“<”),请写出一条能提高二氧化氮转化率的措施。组卷:10引用:3难度:0.5


