2023年人教新版中考化学复习专题:科学探究(1)
发布:2024/9/8 11:0:12
一、选择题
-
1.小丽看到一瓶无色气体,这是什么气体呢?她认为可能是氧气.于是将带火星的木条伸入瓶中,木条复燃.在此过程中,没有应用的科学探究方法是( )
组卷:92引用:5难度:0.7 -
2.某固体在试管中加热后,试管底部没有固体残余物,有关该变化的说法正确的是( )
组卷:55引用:6难度:0.9 -
3.在使用酒精灯的过程中,对下列做法的解释不合理的是( )
组卷:821引用:12难度:0.7 -
4.实验室有如图气体发生装置和气体收集装置:
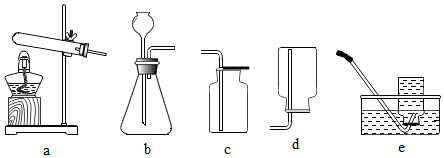
下列说法中,错误的是( )组卷:207引用:5难度:0.3 -
5.在对人体吸入的空气和呼出的气体进行实验探究的过程中,向一瓶空气和一瓶呼出气体中各滴入少量澄清石灰水,振荡,发现只有滴入到呼出气体中的澄清石灰水变浑浊,由此得出的结论是( )
组卷:106引用:22难度:0.7 -
 6.在做测定空气中氧气含量的演示实验中,小亮同学设计如图所示的装置(注射器中装有水,注射器活塞能自由移动),对此装置评价错误的是( )组卷:41引用:3难度:0.7
6.在做测定空气中氧气含量的演示实验中,小亮同学设计如图所示的装置(注射器中装有水,注射器活塞能自由移动),对此装置评价错误的是( )组卷:41引用:3难度:0.7 -
7.下列除杂的试剂和方法不可行的是( )
选项 物质(括号内为杂质) 除杂试剂和方法 A CO2(CO) 通过足量灼热的氧化铜 B FeSO4溶液(CuSO4) 加入过量铁粉,过滤 C NaCl(AgCl) 加足量水溶解、过滤、蒸发结晶 D CuO(C) 加足量稀盐酸,过滤,干燥 组卷:168引用:3难度:0.5
四、科学探究题
-
22.某化学兴趣小组的同学对铜及其化合物进行了相关探究。
Ⅰ.某班同学取用相同总质量的木炭粉和氧化铜的混合物,按图示装置进行实验。实验过程中发现有的小组“黑色固体变红色”这一实验现象不明显。小组同学对此异常现象进行如下探究:
【知识回忆】碳和氧化铜反应的化学方程式为,理论上碳和氧化铜的质量比为。
【作出猜想】产生异常现象可能与所取用木炭粉和氧化铜的质量比有关。
【实验探究】小组同学用总质量相同但质量比不同的木炭粉和氧化铜的混合物(不考虑其中杂质),分别进行实验,部分实验现象记录如下:
【交流讨论】实验序号 m(C):m(CuO) 实验后A处试管中固体颜色 C处导管口的现象 1 1:8 红色固体中有少量黑色固体 尾气燃烧 2 1:9 红色固体中有较少量黑色固体 尾气燃烧 3 1:10 红色固体中有很少量黑色固体 尾气不燃烧 4 1:11 红色固体中有极少量黑色固体 5 1:12 红色固体中无黑色固体 尾气不燃烧 6 1:13 红色固体中有较多黑色固体 尾气不燃烧
①推测实验4中“C处导管口的现象”是。
②上述探究可得出,实验时所用木炭粉和氧化铜的质量比控制在1:10~1:12之间,可观察到黑色固体明显变红,同时还可减少(填化学式)排放,防止空气污染。
【反思评价】分析发现,实验5中m(C):m(CuO)比值与理论值不符,实验后却无黑色固体残留,请用化学方程式解释实验中过量的黑色固体消失的原因:(写一个即可)。
Ⅱ.称取14.4g仅含Cu、O两种元素的固体样品、采用如下装置实验(夹持装置省略),测得实验前后装置B增重4.4g。(碱石灰可以吸收H2O和CO2)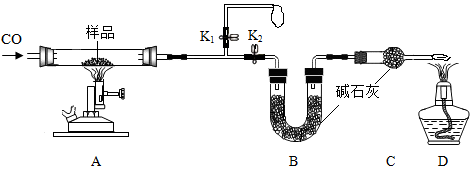
①实验开始前应先关闭,打开。
②装置B的作用是。
③铜元素有多种氧化物,如CuO、Cu2O。根据实验数据进行计算,该固体样品的成分可能是(填序号)
A.Cu2O
B.Cu、CuO
C.CuO、Cu2O
D.Cu、CuO、Cu2O
④若缺少装置C,则实验所得Cu、O个数比(偏大,不变,偏小)。组卷:102引用:4难度:0.2 -
23.过氧化钙(CaO2)是一种重要的化工产品,能杀菌消毒,广泛用于果蔬保鲜、空气净化、污水处理等方面。某兴趣小组同学对其进行了有关探究。
【查阅资料】
(1)过氧化钙是白色、无毒、难溶于水的白色粉末。
(2)2CaO22CaO+O2↑△
(3)CaO2+2HCl═CaCl2+H2O2;二氧化锰与稀盐酸不反应。
【探究1】验证过氧化钙受热分解的产物。
(1)取少量纯净的过氧化钙放入试管中充分加热,将带火星的木条伸入试管,可观察到带火星的木条。
(2)待(1)中试管冷却,取管中少量固体加水充分搅拌,静置,向上层清液中滴加几滴酚酞试液,可观察到溶液变成色。
【探究2】测定产品中过氧化钙的质量分数(假设过氧化钙产品中只含有氧化钙杂质)。
【实验装置】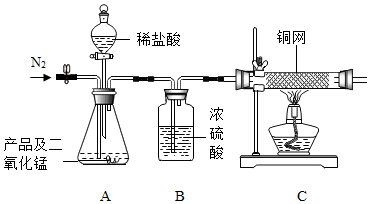
【实验步骤】
①连好装置并检查装置的气密性,在锥形瓶中放入4g该产品;②实验前称量C中铜网的质量;③先缓慢通入氮气,一段时间后加热铜网至红热;再缓慢滴入过量稀盐酸,直至A中样品完全反应;④继续缓慢通入氮气,一段时间后停止加热,待C中铜网冷却后,停止通入氮气;⑤再次称量C中铜网的质量,发现比反应前增重0.8g。
【实验结论】
(1)A中二氧化锰的作用是。
(2)C中铜网发生反应的化学方程式为。
(3)该产品中过氧化钙的质量分数为。
【拓展提升】若A中样品完全反应后,立即停止通氮气并熄灭酒精灯,待C中铜网冷却后称量其质量。你认为该操作对测定产品中过氧化钙的质量分数是否有影响?(选填“是”或“否”,并说明理由)。组卷:104引用:2难度:0.7


