2022-2023学年北京市育才学校高一(下)期中化学试卷
发布:2024/9/9 0:0:8
一、选择题(本题包括20小题,每题只有一个正确选项,每题2分。)
-
1.下列设备工作时,将化学能转化为电能的是( )
A B C D 



锂离子电池 太阳能集热器 燃气灶 硅太阳能电池 组卷:22引用:2难度:0.7 -
2.下列试剂可以用带磨口玻璃瓶塞的试剂瓶保存的是( )
组卷:56引用:8难度:0.9 -
3.下列溶液中,常温下可以用铁罐装运的是( )
组卷:174引用:10难度:0.7 -
4.下列关于SO2性质的说法中,不正确的是( )
组卷:35引用:10难度:0.9 -
5.关于如图所示的原电池,下列说法不正确的是( )
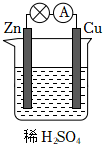 组卷:55引用:3难度:0.9
组卷:55引用:3难度:0.9 -
6.下列有关物质性质与用途具有对应关系的是( )
组卷:80引用:9难度:0.8 -
7.下列实验中的颜色变化,与氧化还原反应无关的是( )
A B C D 实验 NaOH溶液滴入FeSO4溶液中 石蕊溶液滴入氯水中 向CaCl2和氨水的混合液中通入CO2 热铜丝插入稀硝酸中 现象 产生白色沉淀,随后变为红褐色 溶液变红,随后迅速褪色 产生白色沉淀 产生无色气体,随后变为红棕色 组卷:63引用:2难度:0.9 -
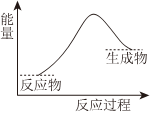 8.下列反应的能量变化能用如图表示的是( )组卷:70引用:1难度:0.7
8.下列反应的能量变化能用如图表示的是( )组卷:70引用:1难度:0.7
二、填空题
-
24.碳酸锂是制备各种锂化合物的关键原料。一种以磷酸锂渣(主要成分Li3PO4)为原料制备碳酸锂的工艺流程示意图如图。
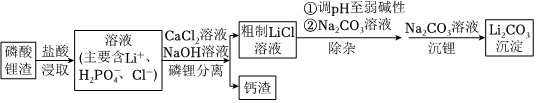
已知:部分物质的溶解性表(20℃)
(1)写出浸取时Li3PO4与盐酸反应的化学方程式:阳离子 阴离子 PO3-4HPO2-4H2 PO-4Li+ 难溶 可溶 易溶 Ca2+ 难溶 难溶 可溶 。
(2)加入盐酸的量不宜过多的原因是。
(3)钙渣的主要成分是。
(4)磷锂分离时,需要不断加入适量NaOH溶液以维持溶液的pH基本不变。结合离子方程式解释其原因是。
(5)沉锂时,反应的离子方程式是。组卷:12引用:1难度:0.6 -
25.某小组同学在实验室制备高铁酸钾(K2FeO4),并探究制备的适宜条件。制备K2FeO4的实验装置如图(夹持装置略)。
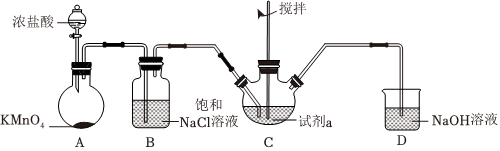
资料:K2FeO4为紫色固体,微溶于KOH溶液。
(1)装置A中产生Cl2的化学方程式是(锰被还原为Mn2+)。
(2)研究试剂a对K2FeO4产率的影响,对比实验如下。
上述实验中,溶液总体积、FeCl3和Fe(NO3)3的物质的量、Cl2的通入量均相同。实验编号 试剂a 实验现象 Ⅰ FeCl3和少量KOH 无明显现象 Ⅱ FeCl3和过量KOH 得到紫色溶液,无紫色固体 Ⅲ Fe(NO3)3和过量KOH 得到紫色溶液(颜色比Ⅱ深),有紫色固体
①实验Ⅱ、Ⅲ产生K2FeO4,将方程式补充完整。
还原反应:。
氧化反应:Fe(OH)3+OH--e-=+FeO2-4。
②对实验Ⅰ未产生K2FeO4而实验Ⅱ能产生的原因提出假设:实验Ⅱ溶液碱性较强,增强+3价铁的还原性。以下实验证实了该假设。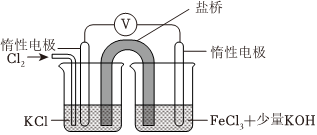
步骤1:通入Cl2,电压表示数为V1;
步骤2:向右侧烧杯中加入(填试剂),电压表示数为V2(V2>V1)。
③反思装置B的作用:用饱和NaCl溶液除去HCl,用平衡移动原理解释。
④实验Ⅱ中K2FeO4的产率比实验Ⅲ低,试解释原因:。
(3)向实验Ⅱ所得紫色溶液中继续通入Cl2,观察到溶液紫色变浅。可能原因是通入Cl2后发生(填离子方程式)而使溶液碱性减弱,进而导致K2FeO4分解。组卷:14引用:1难度:0.5


