2023年江苏省无锡市江阴市南闸中学中考化学二模试卷
发布:2024/7/1 8:0:9
一、选择题(本题包括20小题,每个小题只有一个选项符合题意。1~10题每小题1分,11~20题每小题1分,共30分。)
-
1.下列“阳湖新月”茶叶的部分制作工艺中,主要涉及化学变化的是( )
组卷:28引用:4难度:0.8 -
2.五谷杂粮中的“五谷”通常指的是稻、黍、稷、麦、菽。它们富含的营养物质是( )
组卷:50引用:5难度:0.8 -
3.下列溶液呈中性的是( )
组卷:39引用:1难度:0.8 -
4.北京冬奥会的吉祥物“冰墩墩”内部填充物为聚酯纤维(俗称涤纶)。聚酯纤维属于( )
组卷:53引用:3难度:0.5 -
5.下列关于化学用语的说法正确的是( )
组卷:46引用:2难度:0.5 -
6.浙江大学联合加州大学科研人员,在-50℃环境中,通过静电促使水分子朝电场方向运动,改变其无序的运动状态,从而诱发单晶生长,制成高质量冰单晶微纳光纤。关于冰单晶微纳光纤的说法正确的是( )
组卷:77引用:5难度:0.8 -
7.下列说法中,能体现物质的性质和用途对应关系的是( )
组卷:24引用:1难度:0.7 -
8.肉桂酸甲酯(C10H10O2)常用于调制食用香精,关于肉桂酸甲酯的说法正确的是( )
组卷:30引用:3难度:0.6 -
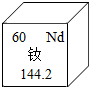 9.在国庆70周年阅兵式上,东风-17导弹首次公开亮相。这款新型常规导弹具备全天候、无依托、强突防的特点,可对中近程目标实施精确打击。导弹之所以有神奇的命中率,是因为制导弹的合金中含有稀土元素钕(Nd)。如图是元素周期表中的钕元素,下列说法错误的是( )组卷:244引用:23难度:0.6
9.在国庆70周年阅兵式上,东风-17导弹首次公开亮相。这款新型常规导弹具备全天候、无依托、强突防的特点,可对中近程目标实施精确打击。导弹之所以有神奇的命中率,是因为制导弹的合金中含有稀土元素钕(Nd)。如图是元素周期表中的钕元素,下列说法错误的是( )组卷:244引用:23难度:0.6
二、非选择题(共50分)
-
27.“自热火锅”中的发热包遇水后可迅速升温至100℃以上,保温时间达2~3小时。兴趣小组对发热包的发热原理及成分进行如下探究。
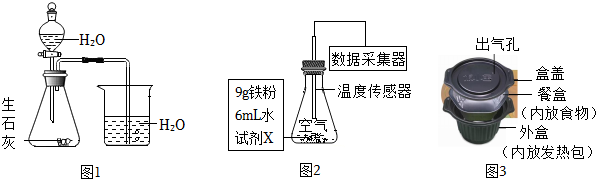
【查阅资料】
①“发热包”主要由生石灰、铁粉、镁粉、铝粉、活性炭、氯化钠组成。
②铝粉与强酸、强碱溶液都能迅速反应生成氢气,同时放出大量热。
Ⅰ.探究发热包的发热原理
【实验探究1】
(1)按图1所示进行实验,加水后,观察到锥形瓶内温度迅速升高,烧杯中(填实验现象);瓶内温度很快下降。
【实验分析1】
生石灰与水反应方程式为。除了该反应放热外,还有其他放热反应存在,如铁粉的锈蚀。
【实验探究2】
为研究铁锈蚀放热的影响因素,用图2所示装置同时进行四组实验,测得实验开始后600s内瓶中温度均呈上升趋势。实验所用试剂X的组成及部分数据如表:
【实验分析2】实验序号 试剂X的组成 温度℃ 活性炭粉/g 食盐/g ① 6 3 35.1℃ ② 6 0 27.9℃ ③ 0 3 23.3℃ ④ 0 0 21.1℃
(2)能证明活性炭粉可加快铁生锈的实验组合有(填实验序号)。
(3)有同学认为实验②、③证明活性炭比食盐对铁粉生锈速率的影响大,请分析该判断是否正确(填“是”或“否”)。
Ⅱ.探究发热包的成分
【实验探究2】
兴趣小组通过如下实验研究发热包的成分:
步骤1:取少量发热包中固体于试管中,加水振荡,静置,滴入几滴酚酞溶液,溶液变为红色。
步骤2:另取少量固体混合物于试管中,逐渐加入稀盐酸至不再产生气泡为止,反应停止后有黑色固体剩余,溶液呈浅绿色。
步骤3:取步骤2所得上层清液少许于另一试管,滴加硝酸银溶液,有白色沉淀生成,继续滴加稀硝酸,沉淀不溶解。
【实验分析3】
(4)“步骤2”中最终溶液变为浅绿色是因为(用化学方程式表示)。
(5)根据以上实验,可确定发热包中一定含有的物质有。
【实验探究4】
(6)若另行设计实验证明该固体混合物中含有铝粉。需选择的试剂是(填序号)。
A.稀盐酸
B.NaOH溶液
C.AgNO3 溶液
【实际运用】
(7)使用图3所示自热米饭时,在外盒禁用热水,若不小心加 入热水,会使得自热米饭盒发生炸裂,请你从微观的角度分析饭盒炸裂的原因:。组卷:96引用:1难度:0.5 -
28.氢氧化钠是重要的化工原料。某兴趣小组对氢氧化钠进行了探究:
Ⅰ.氢氧化钠的制备
用氯化钠溶液制备氢氧化钠的部分流程如图1所示: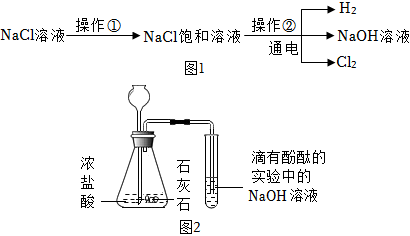
(1)在实验室中进行操作①时,常采取的措施有(任写一种)。
(2)操作②发生反应的化学方程式为。
(3)取少量通过上述流程制得的氢氧化钠样品溶于烧杯中,向其中加入足量氯化钙溶液,有白色沉淀生成,说明样品中含有。
Ⅱ.氢氧化钠的性质
(4)某小组将酚酞溶液滴入NaOH溶液中,溶液变为红色,一段时间后红色消失。
【提出问题】滴有酚酞的NaOH溶液由红色褪为无色的原因是什么?
【猜想与假设】甲同学:酚酞与O2发生了反应。
乙同学:NaOH溶液与空气中的CO2发生了反应。
丙同学:与NaOH溶液浓度大小有关。
【设计与实验】三位同学为验证各自的猜想,设计并进行了如下实验。
①甲同学取少量实验中的NaOH溶液于试管中,加热煮沸,冷却后滴入酚酞溶液,并迅速向试管中滴入植物油,植物油的作用是。
②乙同学进行如图2所示实验,试管中溶液的红色褪去,他认为自己的猜想正确。丁同学认为该现象不能佐证乙同学的猜想,理由是。
③丙同学取质量分数为30%和0.5%的NaOH溶液各2mL分别置于1、2号试管中,滴入相同滴数的酚酞溶液,一段时间后,观察到1号试管中红色褪去,2号试管中,由此判断自己的猜想正确。
Ⅲ.氢氧化钠的应用
(5)“二氧化碳的实验室制取与性质”实验活动产生的废液中含稀盐酸,需先测定其溶质质量分数后进行处理(杂质不参加反应)。
①实验时需配制50g5%的氢氧化钠溶液,若用氢氧化钠固体和水来配制,则需称量氢氧化钠固体的质量为g。
②取20g废液样品于烧杯中,向其中逐滴加入5%的氢氧化钠溶液,恰好完全反应时共消耗氢氧化钠溶液16g。计算废液中盐酸的溶质质量分数(写出计算过程)。
③恰好完全反应时烧杯中的溶液所含粒子数目关系:Na+Cl- (填“>”、“=”或“<”)。组卷:74引用:1难度:0.5


