人教版(2019)选择性必修1《2.1.2 影响化学反应速率的因素 活化能》2023年同步练习卷(4)
发布:2024/8/16 19:0:1
一、选择题
-
1.下列说法错误的是( )
组卷:271引用:4难度:0.9 -
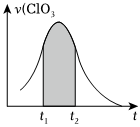 2.KClO3和KHSO3能发生反应:+ClO-3→HSO-3+Cl-+H+(未配平)。已知该反应的速率随c(H+)的增大而加快。如图为用SO2-4在单位时间内物质的量浓度变化表示的该反应υ-t图。下列说法不正确的( )ClO-3组卷:30引用:4难度:0.7
2.KClO3和KHSO3能发生反应:+ClO-3→HSO-3+Cl-+H+(未配平)。已知该反应的速率随c(H+)的增大而加快。如图为用SO2-4在单位时间内物质的量浓度变化表示的该反应υ-t图。下列说法不正确的( )ClO-3组卷:30引用:4难度:0.7 -
3.对处于平衡状态的反应2A(g)+B(g)⇌2C(g)△H<0,下列叙述正确的是( )
组卷:6引用:2难度:0.5 -
4.下列说法不正确的是( )
组卷:9引用:2难度:0.8 -
5.反应3Fe(s)+4H2O(g)
Fe3O4(s)+4H2(g),在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )△组卷:7引用:2难度:0.5
五、解答题
-
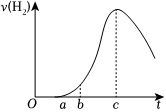 16.把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
16.把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
(1)曲线由O→a段不产生氢气的原因是
有关反应的化学方程式为
(2)曲线a→c段,产生氢气的速率增加较快的主要原因是
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是
(4)该反应若使用催化剂,可使H2产量增多吗?(填“会”或“不会”).组卷:57引用:4难度:0.3 -
17.某学校研究性学习小组设计实验探究铝等金属的性质:将一置于空气中的铝片投入浓氯化铜溶液中,铝片表面出现一层海绵状暗红色物质,接下来铝片上产生大量气泡,产生的气体,具有可燃性,溶液温度迅速上升。若用同样的铝片投入相同浓度的硫酸铜溶液中,在短时间内铝片无明显变化。
(1)铝与氯化铜溶液能迅速反应,而与相同浓度的硫酸铜溶液在短时间内不反应的原因可能是(填序号)。
A.铝与Cl-反应,铝与SO42-不反应
B.氯化铜溶液酸性比同浓度的硫酸铜溶液酸性强
C.生成氯化铝溶于水,而生成硫酸铝不溶于水
D.氯离子能破坏氧化铝表面薄膜,而硫酸根离子不能
请设计一个简单实验验证你的选择:。
(2)铝片表面出现的暗红色物质是,放出的气体是。
(3)某同学为使铝片与硫酸铜溶液反应加快,把铝片投入热氢氧化钠溶液中一段时间后,取出洗涤,再投入硫酸铜溶液中,写出该过程反应的离子方程式。组卷:17引用:2难度:0.7


