2022-2023学年吉林省长春第二实验中学高二(上)期中化学试卷
发布:2024/10/1 2:0:1
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
-
1.下列能量利用过程与化学反应无关的是( )
组卷:2引用:1难度:0.8 -
2.化学与社会、科学、技术、环境密切相关,下列说法错误的是( )
组卷:33引用:4难度:0.7 -
3.化学与生活密切相关,下列与盐类水解无关的是( )
组卷:13引用:6难度:0.6 -
4.下列离子组在由水电离出的氢离子浓度为10-12mol⋅L-1的溶液中,一定不能大量存在的是( )
组卷:8引用:6难度:0.6 -
5.反应Ⅰ:H2(g)+I2(g)⇌2HI(g)的平衡常数为K1;反应Ⅱ:HI(g)⇌
H2(g)+12I2(g)的平衡常数为K2,则K1、K2的关系为(平衡常数为同温度下的测定值( )12组卷:72引用:5难度:0.5 -
 6.如图表示反应2SO2(g)+O2(g)⇌2SO3(g)ΔH<0的正反应速率随时间的变化情况,则t1时刻改变的条件可能是( )组卷:10引用:2难度:0.6
6.如图表示反应2SO2(g)+O2(g)⇌2SO3(g)ΔH<0的正反应速率随时间的变化情况,则t1时刻改变的条件可能是( )组卷:10引用:2难度:0.6
二、非选择题:本题共4小题,共55分。
-
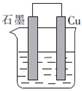 18.含硫和铁的多种化合物可作为原电池材料,按照要求回答下列问题:
18.含硫和铁的多种化合物可作为原电池材料,按照要求回答下列问题:
Ⅰ.依据氧化还原反应2Fe3+(aq)+Cu(s)═Cu2+(aq)+2Fe2+(aq)设计的原电池如图所示。
(1)电解质溶液是(填化学式)溶液。
(2)Cu电极上发生的电极反应为。
(3)石墨电极上发生反应的类型为(填“氧化”或“还原”)反应。
(4)当有1.6g铜溶解时,通过外电路的电子的物质的量为。
Ⅱ.目前锡硫电池的研究获得突破,该电池的总反应是8Sn+S88SnS,放电时其工作原理如图所示。放电充电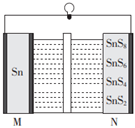
(5)充电时,其能量转化方式为。
(6)放电时,阳离子交换膜中Sn2+向(填“M”或“N”)极移动。
(7)放电时,0.2molSnS6转化为SnS4时,流经导线的电子的物质的量为。组卷:7引用:1难度:0.5 -
19.甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下可合成甲醇,发生的主要反应如下:
Ⅰ.CO(g)+2H2(g)⇌CH3OH(g)ΔH1=-129.0kJ⋅mol-1
Ⅱ.CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH2=+41kJ⋅mol-1
Ⅲ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH3
回答下列问题:
(1)ΔH3=。
(2)将2.0molCO2和3.0molH2通入容积为3L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得H2的平衡转化率与温度的关系如图所示。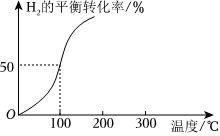
①100℃时反应达到平衡所需的时间为5min,则反应从起始至5min内,用H2表示该反应的平均反应速率为。
②100℃时,反应Ⅱ的平衡常数K=。
③下列可用来判断该反应已达到平衡状态的有(填标号)。
A.CO的含量保持不变
B.容器中c(CO2)=c(CO)
C.容器中混合气体的密度保持不变
D.v正(H2)=v逆(H2O)
(3)利用天然气制取合成气的原理CO2(g)+CH4(g)⇌2CO(g)+2H2(g),在密闭容器中通入物质的量浓度均为1mol⋅L-1的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如图所示,则压强p1p2(填“大于”或“小于”);压强为p2时,在Y点:v(正)v(逆)(填“大于”“小于”或“等于”)。为了提高该反应中CH4的转化率,除温度、压强外还可以采取的措施是。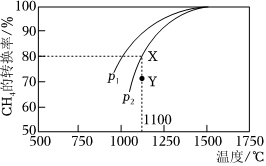 组卷:29引用:4难度:0.4
组卷:29引用:4难度:0.4


