2022-2023学年上海市复旦附中高一(下)期末化学试卷
发布:2024/8/10 2:0:1
一、实现中国梦,离不开金属材料的发展与应用
-
 1.2023年5月,由中国自主研发的C919大型客机开启常态化商业运行。飞机上广泛应用了各种铝合金材料。
1.2023年5月,由中国自主研发的C919大型客机开启常态化商业运行。飞机上广泛应用了各种铝合金材料。
(1)合金具有许多优良的性能,下列物质属于合金的是(双选)。
A.水银
B.青铜
C.生铁
D.黄金
(2)铝合金可以被加工成形状不同的材料,主要是因为其具有良好的性。铝的金属活动性比铁强,空气中铝却比铁具有更好的抗腐蚀性,原因是。
(3)C919大型飞机上使用了大量新型材料铝锂合金,铝锂合金材料的主要优点是:、。
(4)起落架可用铝镁合金制造。合金焊接前需用碱洗,即用NaOH溶液除去铝镁合金表面的自然氧化膜。碱洗时常有气泡冒出,其原因是(用离子方程式表示)。
由我国自主研发的“奋斗者号潜水艇在大平洋马里亚纳海沟成功坐底,创造了中国载人深潜的新纪录。
(5)过氧化钠可用作潜水艇的供氧剂,写出Na2O2和CO2反应的化学方程式:,该反应中生成1mol O2转移的电子数为。
(6)某实验小组通过如图所示实验,探究Na2O2与水的反应,下列说法正确的是。(双选)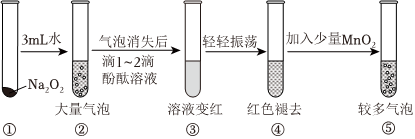
A.②中的大量气泡主要成分是氢气
B.③中溶液变红,说明有酸性物质生成
C.④中现象可能是由于溶液中含有强氧化性物质造成的
D.⑤中MnO2的主要作用是验证溶液中存在过氧化氢
2020年,嫦娥五号的顺利发射,预示着中国对月球的探索更进一步。
月球土壤中富含铁元素,某难溶固体化合物A仅由3种元素组成,科学研究小组按如图流程探究其组成。
已知:A与稀盐酸恰好完全反应,且溶液B只含一种溶质。
(7)固体化合物A所含元素有(填元素符号)。
(8)在有氧条件下,Fe3O4在含Cl-溶液中会转化成固体A且得到的溶液呈碱性,写出该反应的离子方程式。
(9)某同学将上述流程中所得的红棕色固体与一定量H2进行反应,取少许反应后的固体,溶于足量稀盐酸中,再向其中滴加硫氰化钾溶液,溶液未变红。据此,该同学得出结论:此红棕色固体已与H2反应完全。你认为该同学的结论是否严谨?(填“是”或“否”)。请结合离子方程式说明原因。组卷:80引用:1难度:0.5
四、菠菜营养丰富,“大力水手吃了菠菜后变得力大无穷”
-
4.某校化学兴趣小组的同学拟通过实验来探究菠菜中的营养成分。已知信息:
①菠菜中含有草酸,草酸具有还原性。
②菠菜中含有丰富的铁元素,主要以难溶的FeC2O4形式存在,其中铁元素为+2价。
⑧赤血盐K3[Fe(CN)6]用于检验Fe2+,产生特征蓝色沉淀。
Ⅰ.水煮检验法:
(1)操作i中起分离作用的仪器名称为。
(2)溶液A中未能检测出Fe2+的可能原因是。
Ⅱ.灼烧检验法: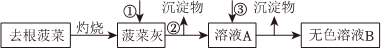
(3)向菠菜灰中加入盐酸浸取后进行操作②,下列操作不规范的有。(双选)
A.玻璃棒用作引流
B.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
C.将滤纸湿润,使其紧贴漏斗壁
D.漏斗末端颈尖未紧靠烧杯内壁
(4)操作⑧加入活性炭的作用是。
(5)甲同学取少量溶液B,滴加酸性KMnO4溶液,振荡后,溶液紫色消失,因此得出结论:溶液B含有Fe2+。乙同学认为甲同学的实验方法不严谨,理由是:。
Ⅱ.分光光度法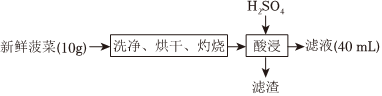
(6)该小组同学利用分光光度法来进行定量测定。已知溶液的吸光度A与溶液中c(Fe3+)关系如图。该小组通过处理上述40mL溶液使其中的铁元素全部转化为Fe3+,从中取出10mL待测液,测得待测液吸光度位于图中X点,试计算菠菜中所含铁元素的含量mg/100g。(结果保留三位小数)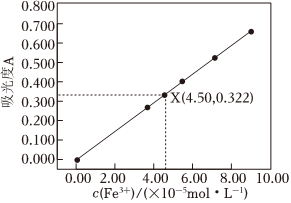 组卷:25引用:1难度:0.5
组卷:25引用:1难度:0.5
五、氮气很稳定,但是它也想变成有用的物质
-
5.含氮化合物在工农业生产过程中的作用举足轻重。人工固氮得到氨气,是人类大规模利用氮元素的起点。
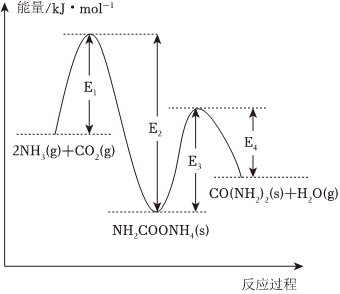
以NH3和CO2为原料合成化肥尿素[CO(NH2)2],两步反应的能量变化如图所示:
(1)已知尿素的熔点为133℃,沸点为197℃,可判断常温下其为晶体,比较熔点高低:CO(NH2)2的熔点(填写“高于”、“低于”或“等于”)NH2COONH4的熔点。
(2)已知第二步反应决定了生产尿素的快慢,可推测E1E3(填“>”、“<”或“=”)。
(3)假设2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g)达到化学平衡后,下列措施能提高NH3转化率的是(双选),该反应的平衡常数表达式K=。
A.选用更有效的催化剂
B.提高氨气的浓度
C.降低反应体系的温度
D.缩小容器的体积
(4)肼(N2H4)-空气燃料电池是一种新型环保型碱性燃料电池,通过氧气与肼反应生成对环境无污染的产物,书写反应的化学方程式并标出电子转移的方向和数目:。
氨的催化氧化过程可发生以下两种反应,该过程易受催化剂选择性影响。
Ⅰ:4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)ΔH<0;
Ⅱ:4NH(g)+3O2(g)⇌2N2(g)+6H2O(g)ΔH<0。
在2L的恒容密闭容器中充入1.5mol NH3和1.55mol O2,一定时间段内,在催化剂作用下发生上述反应。生物NO和N2的物质的量随温度的变化曲线如图所示。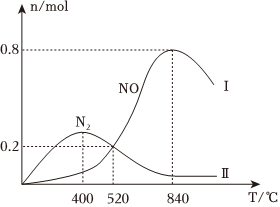
(5)840℃时,仅考虑反应Ⅰ时,NH3的转化率为%。(数字保留2位小数)。
(6)当温度处于400℃~840℃时,温度升高,N2的物质的量减少,NO的物质的量增加,其原因是。
一定条件下,向一恒容密闭容器中通入适量的NO和O2,发生反应:2NO(g)+O2(g)=N2O4(g)。其过程经历两步反应:①2NO(g)+O2(g)=2NO2(g);②2NO2(g)=N2O4(g)。反应体系中NO2、NO、N2O4的浓度(c)随时间的变化曲线如图所示。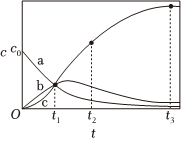
(7)图中曲线a代表的浓度随时间的变化。
(8)图中有一条曲线一定有误,该曲线是(填写字母),理由是。
(9)t2时,c(NO2)的生成速率(填写“大于”、“小于”或者“等于”)消耗速率。
(10)臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g)⇌N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图象作出的判断正确的是(单选)。
A.0~3s内,反应速率为v(O2)=0.2mol/(L•s)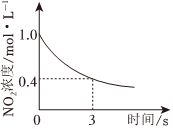
B.达平衡时,仅改变x,则x为c(O2)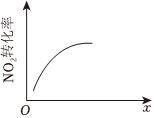
C.t1时仅加入催化剂,平衡正向移动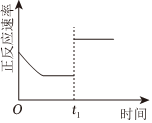
D.升高温度,平衡常数减小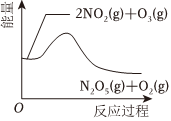 组卷:35引用:1难度:0.5
组卷:35引用:1难度:0.5


