2023年湖北省十一校高考化学第二次联考试卷
发布:2024/5/19 8:0:9
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
-
1.2022年我省重点建设计划超额完成任务。下列相关说法错误的是( )
组卷:31引用:2难度:0.7 -
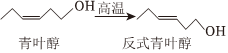 2.茶叶经过高温“杀青”生成清香味的反式青叶醇,转化过程为(如图),下列说法正确的是( )组卷:32引用:2难度:0.7
2.茶叶经过高温“杀青”生成清香味的反式青叶醇,转化过程为(如图),下列说法正确的是( )组卷:32引用:2难度:0.7 -
3.生产生活中蕴藏着丰富的化学知识。下列项目与所述的化学知识没有关联的是( )
选项 项目 化学知识 A 废旧铅酸蓄电池回收PbSO4时加入少量Fe2+ Fe2+可作该反应的催化剂 B 冰在室温下自动熔化成水 冰熔化成水时熵值增大 C 合成氨原料气进入合成塔前需经过铜氨溶液 铜氨溶液可除去CO D BaSO4作“钡餐” BaSO4是强电解质 组卷:17引用:2难度:0.7 -
4.下列离子方程式正确且能准确解释相应实验现象的是( )
组卷:58引用:2难度:0.7 -
5.下列实验操作、现象与结论相匹配的是( )
选项 操作 现象 结论 A 向红热的铁粉与水蒸气反应后的固体中加入稀硫酸酸化,再滴入几滴KSCN溶液 溶液未变红 铁粉与水蒸气未反应 B 常温下,分别测定浓度均为1mol•L-1的CH3COONH4溶液和 NaCl溶液的pH pH均等于7 常温下,1mol•L-1的CH3COONH4溶液和 NaCl溶液中水的电离程度相等 C 常温下,将50mL苯与50mLCH3COOH混合 所得混合溶液的体积为101mL 混合过程中削弱了CH3COOH分子间的氢键,且苯与CH3COOH分子间的作用弱于氢键 D 向CuSO4溶液中滴加浓氨水至过量 先产生蓝色沉淀,后逐渐溶解 Cu(OH)2是两性氢氧化物 组卷:44引用:2难度:0.5 -
6.NA为阿伏加德罗常数的值,下列说法正确的是( )
组卷:23引用:2难度:0.5
二、非选择题:本题共4个小题,共55分。
-
18.电子级氢氟酸是微电子行业的关键性基础材料之一,由萤石粉(主要成分为CaF2,含有少量SiO2和微量As2O3等)制备工艺如图:
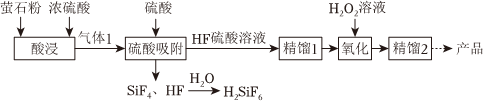
回答下列问题:
(1)“酸浸”时生成HF的化学方程式为,工业生产时往往会适当加热,目的是。
(2)“精馏1”设备使用的材料可选用(填序号)。
A.玻璃
B.陶瓷
C.石英
D.金
(3)已知H2SiF6是一种配位酸,酸性与硝酸相近,可与KMnO4溶液反应制备极易溶于水的强酸HMnO4,反应的离子方程式为。
(4)“氧化”时将AsF3氧化为AsF5。AsF5的沸点高于AsF3,原因是。
(5)液态HF是酸性溶剂,能发生自偶电离:HF⇌H++F-,由于H+和F-都溶剂化,常表示为:3HF⇌H2F++。在HF溶剂中AsF5、BF3呈酸性,HClO3、HNO3、H2O呈碱性,比如AsF5、HClO3的电离方程式分别为:AsF5+2HF⇌HF-2+H2F+;HOClO2+2HF⇌(HO)2ClO++AsF-6。在HF作用下:HF-2
①写出BF3与HNO3反应的离子方程式。
②已知:H2O与AsF5反应生成HAsF6。结合H+的能力:H2O(填“>”、“<”或“=”)。AsF-6组卷:35引用:2难度:0.6 -
19.汽车尾气中含有CO、NO、NO2等大气污染物,可发生以下反应:
①NO2(g)+CO(g)⇌NO(g)+CO2(g)ΔS1=-13.2JK-1⋅mol-1
②2NO(g)+2CO(g)⇌N2(g)+2CO2(g)ΔS2=-197.8JK-1⋅mol-1
③2NO2(g)+4CO(g)⇌N2(g)+4CO2(g)ΔS3
(1)已知ΔG=ΔH-TΔS,(忽略ΔH、ΔS随温度的影响),则ΔS3=J⋅mol-1⋅K。
(2)反应①的平衡常数lgKp~的关系如图1:1T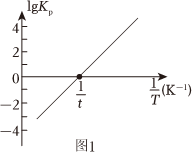
反应①为(填“吸热”或“放热”)反应;温度为tK下,向恒容密闭容器中加入1molCO(g)和1molNO2(g)(若只发生反应①),测得起始压强为20kPa,达到平衡时,NO2的转化率为;NO的分压为kPa。
(3)向体积均为1L的容器中加入2molCO(g)和2molNO(g)(若只发生反应②),其中甲为绝热恒容,乙为恒温恒容,两容器中压强随时间变化曲线如图2: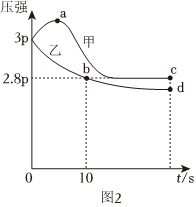
①甲容器中,开始压强增大的原因是。
②c点的逆反应速率大于b点的逆反应速率的原因是。
③c点对应的平衡常数d点对应的平衡常数(填“大于”、“小于”或“等于”)。组卷:30引用:2难度:0.5


