2022-2023学年福建省厦门市思明区湖滨中学九年级(下)期中化学试卷
发布:2024/7/9 8:0:8
一、选择题(每小题只有一个正确选项,1-5题每题2分,6-10题每题3分,共25分)
-
1.端午节吃粽子是传统习俗,在制作粽子的过程中一定发生了化学变化的是( )
组卷:373引用:41难度:0.8 -
2.下列实验操作不正确的是( )
组卷:70引用:8难度:0.9 -
3.下列物质分类正确的是( )
组卷:8引用:2难度:0.8 -
 4.如图为中考化学试卷答题卡中用于识别考生信息的条形码。条形码有黏性,其黏性主要来源于胶黏剂-丙烯酸。丙烯酸的化学式为C3H4O2,下列关于丙烯酸的说法合理的是( )组卷:149引用:5难度:0.5
4.如图为中考化学试卷答题卡中用于识别考生信息的条形码。条形码有黏性,其黏性主要来源于胶黏剂-丙烯酸。丙烯酸的化学式为C3H4O2,下列关于丙烯酸的说法合理的是( )组卷:149引用:5难度:0.5 -
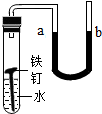 5.如图所示,在盛水的试管中放入一根洁净的铁钉,用带U形管的胶塞塞紧,U型管内水面处于同一高度,一周后观察U型管内水面变化是( )组卷:86引用:17难度:0.9
5.如图所示,在盛水的试管中放入一根洁净的铁钉,用带U形管的胶塞塞紧,U型管内水面处于同一高度,一周后观察U型管内水面变化是( )组卷:86引用:17难度:0.9
二、非选择题
-
16.现有平板电视显示屏工厂生产过程中丢弃废玻璃粉末(含SiO2、Fe2O3、CeO2等物质),某课题组以此粉末为原料回收铈和硫酸亚铁晶体,设计实验流程如下:
资料1:CeO2是一种金属氧化物,化学性质稳定,与稀硫酸不反应。在H2O2存在的条件下,两种物质能反应。
资料2:FeSO4容易被空气中的O2氧化。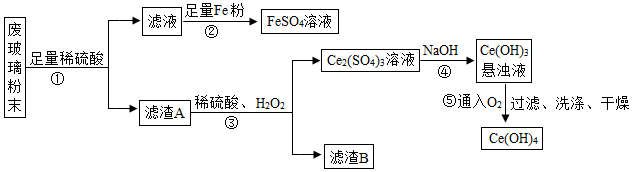
(1)写出①反应的化学方程式,该反应类型为,为提高①中的反应效率,可采用的具体措施有。(写一种即可)
(2)将②中所得FeSO4溶液在氮气环境中蒸发浓缩、、过滤,得到FeSO4晶体,其中氮气的作用是。
(3)请补充完整③反应的化学方程式:2CeO2+3H2SO4+H2O2═Ce2(SO4)3++O2↑,滤渣B的主要成分是。
(4)生产过程中可循环利用的物质是。
(5)Ce(OH)4中的Ce元素化合价为价。组卷:73引用:3难度:0.4 -
17.碳酸氢钠是应用广泛的盐,化学小组对其进行了探究。
(一)碳酸氢钠的制备
【查阅资料】Ⅰ.侯氏制碱的原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;2NaHCO3Na2CO3+H2O+CO2↑。△
Ⅱ.研究发现:NaHCO3溶于水时吸收热量,Na2CO3溶于水时放出热量。
【实验制备】根据侯氏制碱原理设计,用图甲装置制取NaHCO3。反应结束后,将试管中的混合物过滤、洗涤、低温烘干得到白色固体。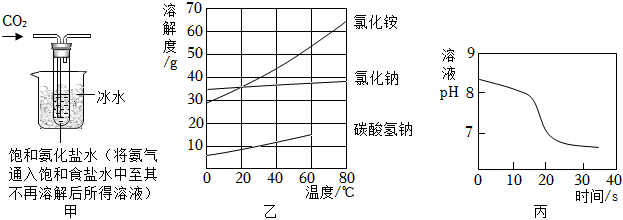
(1)烧杯中冰水的作用是。
(2)能进一步确认该白色固体是NaHCO3的可行方案是(填字母序号)。
A.取少量白色固体于试管中,滴加稀盐酸,若有气泡,则固体是NaHCO3
B.取少量白色固体于试管中,加水溶解,并用温度计测量温度变化,若温度计示数下降,则固体是NaHCO3
(3)图乙中碳酸氢钠的溶解度在60℃后无数据的原因可能是。
【性质探究】
常温下,取一定量的NaHCO3溶液于烧杯中,插入pH传感器,向烧杯中持续滴加CaCl2溶液,有白色沉淀生成,当溶液的pH变为6.68时开始有无色气体产生。反应过程中溶液的pH随时间变化如图丙。
【交流反思】
(4)NaHCO3溶液显(填“酸”“碱”或“中”)性。
(二)测定碳酸氢钠的含量
已知制得的碳酸氢钠样品中含有少量氯化钠,某探究小组欲测定该碳酸氢钠的纯度。
【实验步骤】
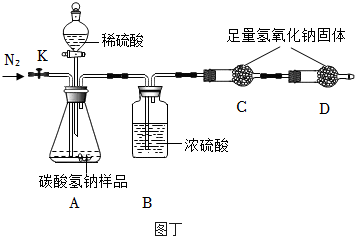
(5)①组装如图装置,并;
②称取一定量的样品放入锥形瓶中,加少量水溶解,并在其他装置中加入相应的药品;
③打开止水夹K,缓缓通入一段时间N2后关闭K,称取装置C的质量;
④打开分液漏斗的旋塞滴入稀硫酸,直到不在产生气泡为止;
⑤再次打开止水夹K,缓缓通入一段时间N2,再次称量装置C的质量。
【实验分析】
(6)B装置的作用是。
(7)步骤⑤中缓缓通入一段时间N2的目的是。
(8)如果缺少装置D,所测样品中碳酸氢钠的质量分数(填“偏大”“偏小”或“不变”)。
(9)取10g碳酸氢钠固体样品于锥形瓶中,加入足量的稀硫酸,若C处固体增重4.4g,计算样品中碳酸氢钠的质量分数。
提示:本实验的化学方程式为:2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O。组卷:26引用:2难度:0.4


