2023年天津市塘沽一中等12校高考化学联考试卷(二)
发布:2024/5/12 8:0:9
一、选择题(共12小题,每小题3分,满分36分)
-
1.化学与生活息息相关,下列有关说法正确的是( )
组卷:58引用:1难度:0.6 -
2.下列有关化学用语表示正确的是( )
组卷:40引用:1难度:0.5 -
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
组卷:88引用:1难度:0.6 -
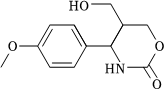 4.某有机物的结构如图所示,关于该有机物下列说法错误的是( )组卷:56引用:2难度:0.5
4.某有机物的结构如图所示,关于该有机物下列说法错误的是( )组卷:56引用:2难度:0.5 -
5.下列说法正确的是( )
组卷:102引用:2难度:0.5
二、解答题(共4小题,满分64分)
-
15.实验室利用SO2合成硫酰氯(SO2Cl2),并对H2SO3和HClO的酸性强弱进行探究。可利用SO2与Cl2在活性炭作用下反应,制取少量的SO2Cl2,反应原理为:SO2(g)+Cl2(g)=SO2Cl2(l)ΔH<0。如图所示(部分夹持装置省略)。已知:SO2Cl2的熔点为-54.1℃,沸点为69.1℃,100℃以上易分解,遇水能剧烈反应,产生白雾。
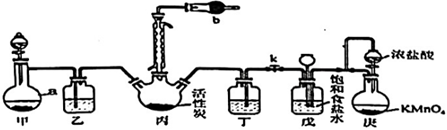
(1)甲装置用于制SO2,则下列试剂组合中最合适的是。(填序号)
A.18.4mol⋅L-1的硫酸和Al
B.5mol⋅L-1的硝酸和Na2SO3固体
C.10mol⋅L-1的硫酸和Na2SO3固体
D.0.5mol⋅L-1的硫酸和Na2SO3固体
(2)装置乙和丁中可以使用同一种试剂,该试剂为(写名称)。若缺少装置乙和丁,对产品硫酰氯会有何影响,请用化学方程式表示。
(3)仪器a的名称是,仪器b中盛放的试剂的作用是,装置戊中长颈漏斗的作用是。
(4)反应过程中,为防止SO2Cl2分解,可采取的措施有(至少写一条)。
(5)少量硫酰氯也可用氯磺酸(ClSO2H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。
①从分解产物中分离出硫酰氯的实验操作名称为。
②设计实验检验氯磺酸分解制取硫酰氯产品中混有硫酸,合理的是:(填字母)。
A.取样品溶于水,滴加紫色石蕊溶液变红:再取少量溶液,加入BaCl2溶液产生白色沉淀,说明含有H2SO4。
B.取样品在干燥条件下加热至完全反应,冷却后直接加BaCl2溶液,有白色沉淀,再滴加紫色石蕊溶液变红,说明含有H2SO4。
(6)选用下面的装置探究酸性:H2SO3>HClO,其连接顺序为A→。能证明H2SO3的酸性强于HClO的实验现象为。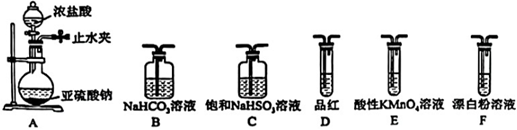 组卷:104引用:1难度:0.5
组卷:104引用:1难度:0.5 -
16.碳及其化合物是重要的化工原料,但对气候环境造成不良影响,需要综合利用。
(1)工业上利用如下反应制H2:CO(g)+H2O(g)⇌CO2(g)+H2(g)ΔH2=-41.2kJ⋅mol-1。
①在不同进气比和不同温度下(其他条件相同),测得相应的CO平衡转化率见表。
a点平衡混合物中H2的体积分数平衡点 a b c n(CO):n(H2O) 0.5 0.5 1 CO平衡转化率/% 50 66.7 50 (保留3位有效数字),a、c两点对应的反应温度TaTc(填“<”“=”或“>”)。
②若在恒容绝热的密闭容器中通入一定量的CO和H2O发生此反应,下列说法表示该反应达到最大限度的是(填标号)。
a.装置内的气体无CO
b.装置内的压强不再变化
c.H2的体积分数不变
d.装置内气体摩尔质量不变
③一定温度下,在3L容积可变的密闭容器中发生该反应,已知c(CO)随时间t的变化曲线a如图1所示,在t1时刻改变一个条件,曲线a变为b,则改变的条件是。
(2)甲烷可用于制备合成气:CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH。将CH4(g)和H2O(g)以物质的量之比为1:3充入盛有催化剂的刚性容器中发生该反应。相同时间段内测得CO的体积分数(ϕ)与温度(T)的关系如图2所示。T0℃时,CO的体积分数最大的原因为。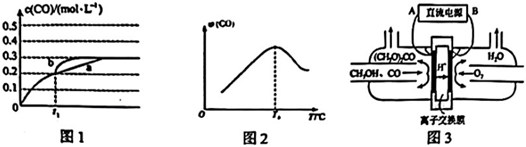
(3)以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图3所示。阳极的电极反应式为。
(4)工业废气中的CO2可用氨水捕获生成NH4HCO3溶液。常温下NH4HCO3溶液中:c()NH+4c()(填“>”、“<”或“=”);HCO-3+NH+4+H2O⇌NH3⋅H2O+H2CO3的平衡常数K=HCO-3。(已知常温下NH3⋅H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7mol⋅L-1、K2=4×10-11mol⋅L-1)组卷:71引用:1难度:0.5


