2023年湖北省武汉市武昌实验中学高考化学适应性试卷
发布:2024/6/1 8:0:9
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只
-
1.2023年湖北省生态环境保护工作会议要求切实扛起美丽湖北建设的历史使命,下列行为不符合该主题的是( )
组卷:59引用:1难度:0.7 -
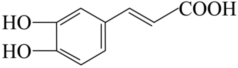 2.咖啡中含有的咖啡酸(结构如图)能使人心脑血管更年轻。下列有关咖啡酸的叙述不正确的是( )组卷:41引用:1难度:0.7
2.咖啡中含有的咖啡酸(结构如图)能使人心脑血管更年轻。下列有关咖啡酸的叙述不正确的是( )组卷:41引用:1难度:0.7 -
3.中华传统文化蕴含着丰富的化学知识,下述之物见其还原性者( )
组卷:135引用:2难度:0.7 -
4.下列离子方程式正确的是( )
组卷:61引用:1难度:0.6 -
5.下列物质与用途对应不正确的是( )
组卷:52引用:1难度:0.7 -
6.下列实验操作正确且能达到实验目的的是( )
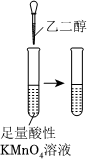
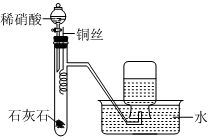
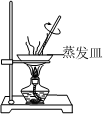
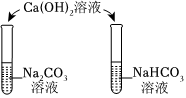
A.将乙二醇转化为乙二酸 B.验证稀硝酸的还原产物为NO C.除去NaCl固体中的NH4Cl D.鉴别NaHCO3溶液和Na2CO3溶液 组卷:52引用:1难度:0.5
二、非选择题:本题共4小题,共55分。
-
18.氮化镓(GaN)具有优异的光电性能。一种利用炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4、SiO2]制备GaN的工艺流程如图:
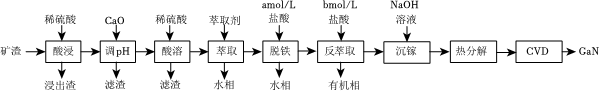
已知:
①常温下,Ksp[Zn(OH)2]=10-16.6,Ksp[Ga(OH)3]=10-35.1,Ksp[Fe(OH)3]=10-38.5。
②Ga3+、Fe3+在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
回答下列问题:盐酸浓度/mol⋅L-1 反萃取率/% Ga3+ Fe3+ 2 86.9 9.4 4 69.1 52.1 6 17.5 71.3
(1)“酸浸”时Ga2(Fe2O4)3发生反应的离子方程式为。“酸溶”所得滤渣的主要成分是(填化学式)。
(2)“酸浸”所得浸出液中Ga3+、Zn2+浓度分别为0.21g•L-1、65g•L-1。常温下,为尽可能多地提取Ga3+并确保不混入Zn(OH)2,“调pH”时需用CaO将pH增大至接近(假设调pH时溶液体积不变)。
(3)“脱铁”和“反萃取”时,所用盐酸的浓度a=,b=(选填上表中盐酸的浓度)。
(4)“沉镓”时,若加入NaOH的量过多,会导致Ga3+的沉淀率降低,原因是(用离子方程式表示)。
(5)利用CVD(化学气相沉积)技术,将热分解得到的Ga2O3与NH3在高温下反应可制得GaN,同时生成另一种产物,该反应化学方程式为。组卷:52引用:1难度:0.5 -
19.除去废水中Cr(Ⅵ)的方法有多种。请按要求回答下列问题。
(1)室温下,含Cr(Ⅵ)的微粒在水溶液中存在如下平衡:
H2CrO4(aq)⇌H+(aq)+(aq)△H1HCrO-4(aq)⇌H+(aq)+HCrO-4(aq)△H2CrO2-4
2(aq)⇌Cr2HCrO-4(aq)+H2O(l)△H3O2-7
①室温下,反应2(aq)+2H+(aq)⇌Cr2CrO2-4(aq)+H2O(l) 的△H=O2-7(用含△H1、△H2或△H3的代数式表示)。
②室温下,初始浓度为1.0mol•L-1的Na2CrO4溶液中c(Cr2)随c(H+)的变化如图所示。O2-7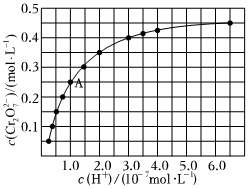
根据A点数据计算反应2+2H+⇌Cr2CrO2-4+H2O 的K=O2-7,下列关于该反应的说法不正确的是。
A.加水稀释,平衡右移,K值增大
B.若达到A点的时间为5s,则v()=0.1mol•L-1•s-1CrO2-4
C.若升高温度,溶液中的平衡转化率减小,则该反应的△H>0CrO2-4
(2)NaHSO3与熟石灰除Cr(Ⅵ)法:向酸性废水中加入NaHSO3,再加入熟石灰,使Cr3+沉淀。
①实验中的NaHSO3作用是。
②Cr(Ⅲ)在水溶液中的存在形态分布如图1所示。当pH>12时,Cr(Ⅲ)去除率下降的原因可用离子方程式表示为。
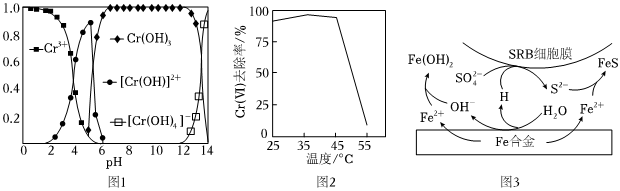
(3)微生物法:
①用硫酸盐还原菌(SRB)处理含Cr(Ⅵ)废水时,Cr(Ⅵ)去除率随温度的变化如图2所示。55℃时,Cr(Ⅵ)的去除率很低的原因是。
②水体中,Fe合金在SRB存在条件下腐蚀的机理如图3所示。Fe腐蚀后生成FeS的过程可描述为:Fe失去电子转化为Fe2+,H2O得到电子转化为H,。组卷:52引用:1难度:0.6


