2022-2023学年北京市101中学高一(下)期末化学试卷(等级考)
发布:2024/7/3 8:0:9
一、(共14道小题,每小题只有一个选项符合题意,每小题3分.)
-
1.下列设备工作时,将化学能转化为电能的是( )
A B C D 



碱性干电池 风力发电机 太阳能集热器 燃气灶 组卷:39引用:2难度:0.7 -
2.下列物质中属于含有共价键的强电解质的是( )
组卷:89引用:2难度:0.8 -
3.我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程,该历程示意图如图所示。
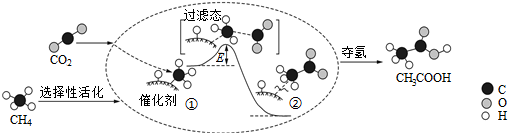
下列说法不正确的是( )组卷:138引用:36难度:0.7 -
4.下列有关原电池装置的说法不正确的是( )
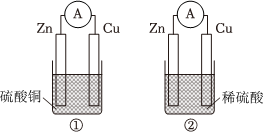 组卷:73引用:3难度:0.7
组卷:73引用:3难度:0.7 -
5.某有机物的结构如图所示,则下列说法正确的是( )
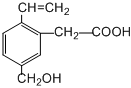 组卷:45引用:7难度:0.7
组卷:45引用:7难度:0.7 -
6.由N2O和NO反应生成N2和NO2的能量变化如图所示。下列说法不正确的是( )
 组卷:89引用:9难度:0.7
组卷:89引用:9难度:0.7
Ⅱ卷;非选择题(共58分)
-
18.铁及其化合物在日常生活中有广泛应用.
(1)写出Fe(OH)2转化为Fe(OH)3的化学方程式.
(2)绿矾(FeSO4•7H2O)是补血剂的原料,易变质.检验绿矾是否变质的试剂是设计实验检验绿矾是否完全变质
(3)利用绿矾制备还原铁粉的工业流程如图1: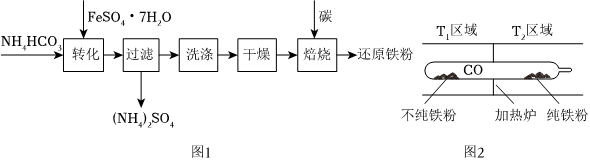
①干燥过程主要是为了脱去游离水和结晶水,过程中会有少量FeCO3•nH2O在空气中被氧化为FeOOH,该反应的化学方程式为
②取干燥后的FeCO3样品12.49g,焙烧,最终得到还原铁粉6.16g,计算样品中杂质FeOOH的质量
(4)以羰基化合物为载体运用化学平衡移动原理分离、提纯某纳米级活性铁粉(含有一些不反应的杂质),反应装置如图2.Fe(s)+5CO(g)⇌Fe(CO)5(g)△H<0
T1T2(填“>”、“<”或“=”),判断理由是.组卷:42引用:3难度:0.5 -
19.已知FeCl3溶液与KI溶液的反应为可逆反应,某小组同学对该反应进行实验探究.
(1)甲同学首先进行了实验1.
①写出FeCl3溶液与KI溶液反应的离子方程式实验
1实验步骤 实验现象 ⅰ.取2mL 1mol•L-1 KI溶液,滴加0.1mol•L-1 FeCl3溶液3滴(1滴约为0.05mL,下同). ⅰ.溶液呈棕黄色. ⅱ.向其中滴加2滴0.1mol•L-1 KSCN溶液. ⅱ.溶液不显红色. .
②加入KSCN溶液的目的是.
③甲同学认为溶液不显红色的原因是反应体系中c(Fe3+)太低,故改进实验方案,进行了实验2.
本实验改用0.1mol•L-1 KI溶液的目的是实验
2实验步骤 实验现象 ⅰ.取2mL 0.1mol•L-1 KI溶液,滴加0.1mol•L-1 FeCl3溶液3滴. ⅰ.溶液呈棕黄色. ⅱ.向其中滴加2滴0.1mol•L-1 KSCN溶液. ⅱ.溶液显红色. ⅲ.继续加入2mL CCl4,充分振荡、静置. ⅲ.液体分层,上层红色消失,变为棕黄色,下层呈紫红色. .用化学平衡原理解释实验2中加入CCl4后上层溶液红色消失的原因:.
(2)甲同学认为“用CCl4萃取后上层溶液仍为棕黄色”的原因是I2未被充分萃取,但乙同学查阅资料得到信息:I2、I3-在水中均呈棕黄色,两者有如下关系:I2+I-⇌I3-.于是提出假设:萃取后的溶液呈棕黄色的主要原因是存在I3-.
①为验证假设,乙同学设计并完成了实验3.
实验3的结论是实验3 实验步骤 实验现象 ⅰ.取1mL实验2中棕黄色的上层清液,再加入2mL CCl4,振荡、静置. ⅰ.液体分层,上层呈黄色,下层呈紫红色. ⅱ.取1mL饱和碘水,加入2mL CCl4,振荡、静置. ⅱ.液体分层,上层为无色,下层呈紫红色. .
②甲同学依据乙同学的实验设计思路,选用实验2中的试剂,运用控制变量的方法设计了更加严谨的实验,证明了平衡I2+I-⇌I3-的存在.
请你补充完整他设计的实验步骤:将实验2中下层紫红色溶液平均分成两份,分装于两支试管中,向试管1中加入1mL水,振荡、静置;向试管2中.
两支试管中的现象分别为.组卷:213引用:9难度:0.5


