2021年江苏省苏州市高新区中考化学二模试卷
发布:2024/5/8 8:0:8
一、单选题
-
1.《天工开物》是我国古代科技发展的智慧结晶,书中描述的下列制瓷工序涉及化学变化的是( )
组卷:585引用:69难度:0.9 -
2.走绿色发展道路,既要金山银山又要绿水青山。下列关于环境方面的知识正确的是( )
组卷:205引用:13难度:0.5 -
3.下列位置或场所的标识,错误的是( )




A.存放浓硫酸的试剂柜 B.运输酒精的槽罐车 C.面粉加工厂 D.居民住宅区 组卷:40引用:4难度:0.7 -
4.下列实验操作正确的是( )
组卷:61引用:5难度:0.7 -
5.分类是一种重要的研究方法。以下对常见物质的分类正确的是( )
组卷:50引用:5难度:0.7 -
6.下列物质的用途及其依据的性质均正确的是( )
组卷:42引用:6难度:0.8 -
7.下列“家庭小实验”不能达到预期目的是( )
组卷:33引用:3难度:0.7 -
8.下列物质由离子构成的是( )
组卷:190引用:17难度:0.6 -
9.纳米铁粉在空气中能自燃并生成一种红色氧化物。对比铁丝在空气中不能燃烧,而在氧气中能剧烈燃烧的事实,某同学得出的下列结论不正确的是( )
组卷:1325引用:71难度:0.7
七、科学探究题
-
27.绿矾(FeSO4•7H2O),在医药、净水、化肥、农药等方面有广泛的应用。化学小组的同学在用绿矾配制FeSO4溶液时发现,溶液颜色会由绿变黄,于是开展了以下探究活动。
【查阅资料】
i.FeSO4溶液如果长时间显露在空气中,会与氧气发生反应转换成Fe2(SO4)3,色泽由最初的浅绿色或淡绿色转变成黄色。反应生成的Fe2(SO4)3遇KSCN溶液会变红。
ii.保存FeSO4溶液时要加入稀硫酸和铁钉,置于阴凉处。
【提出猜想】
影响FeSO4溶液与氧气反应速率的因素可能有温度、浓度、溶液酸碱性、是否有铁钉等。
【进行实验】
【解释与结论】编号 实验 0min 30min 2h ① 
溶液为浅绿色 溶液略显黄色 溶液黄色略有加深 ② 
溶液为浅绿色 溶液明显变黄 溶液黄色明显加深 ③ 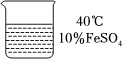
溶液立即变黄 ④ 
溶液为浅绿色 溶液明显变黄,振荡后无变化 溶液黄色明显加深,振荡无变化 ⑤ 
溶液为浅绿色 溶液为浅绿色 溶液为浅绿色;滴加KSCN溶液后,略显红色 ⑥ 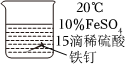
溶液为浅绿色 溶液为浅绿色 溶液为浅绿色;滴加KSCN溶液后,略显红色,振荡后溶液变为浅绿色
(1)FeSO4溶液为浅绿色或淡绿色,Fe2(SO4)3溶液为黄色,可见这两种盐溶液的颜色差异与元素有关。
(2)实验①中实验温度T=℃。
(3)通过对比实验②和③,得出的结论是。
(4)欲得出“稀硫酸和铁钉共同存在下才能有效防止FeSO4溶液变质”的结论,需要对比(填写实验编号)。
(5)写出实验⑤中,FeSO4溶液变质的化学方程式。
(6)下列说法正确的是。
A.其他条件相同,溶液酸性增强,FeSO4溶液变质加快
B.其他条件相同,FeSO4溶液浓度越大,变质越快
C.实验⑥中,滴加KSCN溶液后,略显红色,振荡后溶液变为浅绿色,可能是发生了反应组卷:13引用:1难度:0.6
八、计算题
-
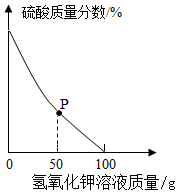 28.取某酸性废水样品100g,逐滴加入5.6%的氢氧化钾溶液,废水中硫酸的质量分数变化如图所示。(假设废水中其他成分不与氢氧化钾反应且不含硫酸钾)
28.取某酸性废水样品100g,逐滴加入5.6%的氢氧化钾溶液,废水中硫酸的质量分数变化如图所示。(假设废水中其他成分不与氢氧化钾反应且不含硫酸钾)
(1)P点对应溶液中一定存在的阳离子有(填离子符号)。
(2)酸性废水中硫酸的质量分数为(用百分数表示,保留到0.1%)。
(3)计算当废水处理至中性时,溶液中硫酸钾的质量分数(写出计算过程,结果用百分数表示保留到0.1%)。组卷:45引用:3难度:0.5


