人教版(2019)选择性必修1《第2章 化学反应速率与化学平衡》2023年单元测试卷(1)(2)
发布:2024/8/16 7:0:3
一、选择题
-
1.化学在日常生活和生产中有着重要的应用.下列说法不正确的是( )
组卷:30引用:5难度:0.9 -
2.CH3COOH与CH3COONa等物质的量混合配制成稀溶液,pH为4.7,下列说法错误的是( )
组卷:59引用:9难度:0.5 -
3.往锅炉注入Na2CO3溶液浸泡,将水垢中的CaSO4转化为CaCO3,再用盐酸去除,下列叙述正确的是( )
组卷:85引用:5难度:0.5 -
4.室温下,在一定体积pH=12的Ba(OH)2溶液中逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若体积可以加和,则V(Ba(OH)2):V( NaHSO4)为( )
组卷:88引用:6难度:0.5
三、解答题
-
 11.三氯氧磷(POCl3)广泛用于农药、医药等生产。工业制备三氯氧磷的过程中会产生副产品亚磷酸(H3PO3)。回答下列问题:
11.三氯氧磷(POCl3)广泛用于农药、医药等生产。工业制备三氯氧磷的过程中会产生副产品亚磷酸(H3PO3)。回答下列问题:
(1)三氯氧磷可由三氯化磷、水、氯气加热反应生成,反应的化学方程式为。
(2)已知亚磷酸(H3PO3)为二元弱酸,则Na2HPO3溶液中,各离子浓度的大小关系为。
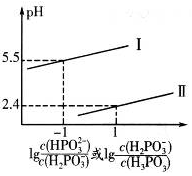
(3)常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示1g的是曲线c(HPO2-3)c(H2PO-3)(填“I”或“Ⅱ”),亚磷酸(H3PO3)的Ka1=mol•L-1,反应HPO32-+H2O⇌H2PO3-+OH-的平衡常数的值是。
(4)工业上生产三氯氧磷的同时会产生含磷废水(主要成分为H3PO4、H3PO3)。向废水中先加入适量漂白粉,再加入生石灰调节pH,将磷元素转化为磷酸的钙盐沉淀并回收。若处理后的废水中c(Ca2+)=5×10-6mol•L-1,则溶液中c(PO43-)=mol•L-1.(已知Ksp[Ca3(PO4)2]=2×10-29)组卷:322引用:3难度:0.1 -
12.NO和SO2等气体都是大气污染物,对它们的治理具有重要意义。某研究小组利用稀土金属铈(Ce)吸收NO,同时获得Na2S2O4和NH4NO3的工艺流程如图所示,回答相关问题:
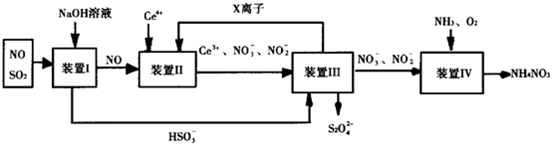
(1)实验室配制1000mL 2.0mol•L-1NaOH溶液,需要的玻璃仪器有烧杯、玻璃棒、胶头滴管、;写出装置Ⅰ中发生的主要化学方程式。
(2)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式。
(3)装置Ⅲ是电解槽,从中得到的X表示(填离子符号);S2O42-是(填“氧化”或“还原”)产物。
(4)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g•L-1,要使1L该溶液中的NO2-完全转化为NH4NO3,至少需向装置Ⅳ中通入标准状况下的氧气L(用含a的代数式表示,保留小数点后3位)。组卷:10引用:3难度:0.5


