2022-2023学年福建省厦门市集美中学高三(上)期中化学试卷
发布:2024/9/13 0:0:8
一、选择题(每题只有一个正确选项,16题,共48分)
-
1.生活中处处有化学,下列叙述正确的是( )
组卷:52引用:9难度:0.7 -
2.反应NH4Cl+NaNO2═NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是( )
组卷:740引用:39难度:0.7 -
3.宋代《千里江山图)描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料[主要成分为Cu(OH)2•CuCO3],青色来自蓝铜矿颜料[主要成分为Cu(OH)2•2CuCO3]。下列说法错误的是( )
组卷:823引用:29难度:0.6 -
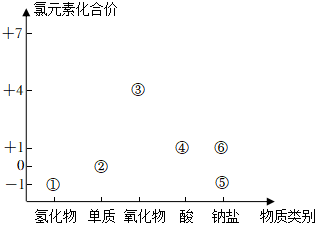 4.价类二维图是学习元素及其化合物知识的重要模型。它是以元素化合价为纵坐标,以物质类别为横坐标的二维平面图象。如图为氯元素的价类二维图。下列叙述不正确的是( )组卷:54引用:3难度:0.6
4.价类二维图是学习元素及其化合物知识的重要模型。它是以元素化合价为纵坐标,以物质类别为横坐标的二维平面图象。如图为氯元素的价类二维图。下列叙述不正确的是( )组卷:54引用:3难度:0.6 -
5.常温下,下列各组离子在指定溶液中能大量共存的是( )
组卷:1418引用:20难度:0.5 -
6.雄黄(As4S4,
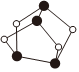 )与雌黄(As2S3)在古代均曾入药。二者可发生如图转化;NA表示阿伏加德罗常数的值,下列说法正确的是( )
)与雌黄(As2S3)在古代均曾入药。二者可发生如图转化;NA表示阿伏加德罗常数的值,下列说法正确的是( )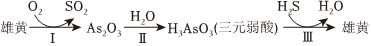 组卷:18引用:4难度:0.7
组卷:18引用:4难度:0.7
二、非选择题(4题,共52分)
-
19.稀土(RE)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如图:
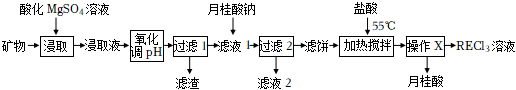
已知:月桂酸(C11H23COOH)熔点为44℃;月桂酸和(C11H23COO)3RE均难溶于水。该工艺条件下,稀土离子保持+3价不变;(C11H23COO)2Mg的Ksp=1.8×10-8;Al(OH)3开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。
(1)“氧化调pH”中,化合价有变化的金属离子是离子 Mg2+ Fe3+ Al3+ RE3+ 开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4 沉淀完全时的pH / 3.2 4.7 / 。
(2)“过滤1”前,用NaOH溶液调pH至的范围内,该过程中Al3+发生反应的离子方程式为。
(3)“过滤2”后,滤饼中检测不到Mg元素,滤液2中Mg2+浓度为2.7g•L-1。为尽可能多地提取RE3+,可提高月桂酸钠的加入量,但应确保“过滤2”前的溶液中c(C11H23COO-)低于mol•L-1(保留两位有效数字)。
(4)①“加热搅拌”有利于加快RE3+溶出、提高产率,其原因是。
②“操作X”的过程为:先,再固液分离。
(5)该工艺中,可再生循环利用的物质有(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂Pt3Y。
①还原YCl3和PtCl4熔融盐制备Pt3Y时,生成1molPt3Y转移mol电子。
②Pt3Y/C用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化O2的还原,发生的电极反应为。组卷:689引用:4难度:0.3 -
20.金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途。目前生产钛的方法之一是将金红石(TiO2)转化为TiCl4,再进一步还原得到钛。回答下列问题:
(1)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
(ⅰ)直接氯化:TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g)ΔH1=172kJ•mol-1,Kp1=1.0×10-2
(ⅱ)碳氯化:TiO2(s)+2Cl2(g)+2C(s)═TiCl4(g)+2CO(g)ΔH2=-51kJ•mol-1,Kp2=1.2×1012Pa
①反应2C(s)+O2(g)═2CO(g)的ΔH为kJ•mol-1,Kp=Pa。
②碳氯化的反应趋势远大于直接氯化,其原因是。
③对于碳氯化反应:增大压强,平衡移动(填“向左”“向右”或“不”);温度升高,平衡转化率(填“变大”“变小”或“不变”)。
(2)在1.0×105Pa,将TiO2、C、Cl2以物质的量比1:2.2:2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。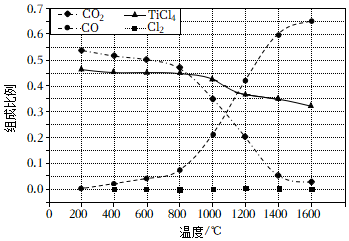
①反应C(s)+CO2(g)═2CO(g)的平衡常数Kp(1400℃)=Pa。
②图中显示,在200℃平衡时TiO2几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是。
(3)TiO2碳氯化是一个“气-固-固”反应,有利于TiO2-C“固-固”接触的措施是。组卷:973引用:3难度:0.5


