2023-2024学年广东省广州市培英中学高二(上)期中化学试卷
发布:2024/9/28 3:0:4
一、选择题:本题共16小题,第1~10题每小题2分;第11~16题每小题2分,共44分。在每小题给出的四个选项中,只有一项是符合题目要求的。
-
1.在测定中和反应反应热的实验中,下列说法正确的是( )
组卷:24引用:1难度:0.7 -
2.下列事实中,能用勒夏特列原理解释的是( )
①夏天,打开啤酒瓶时会从瓶口逸出气体
②浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体
③实验室可用排饱和食盐水的方法收集氯气
④将盛有二氧化氮和四氧化二氮混合气体的密闭容器置于冷水中,混合气体的颜色变浅
⑤使用催化剂可加快SO2转化为SO3的速率
⑥合成氨时,将氨液化分离,可提高原料利用率组卷:54引用:2难度:0.7 -
3.在0.1mol/L的NH3•H2O溶液中存在如下电离平衡:NH3•H2O⇌
+OH-对于该平衡,下列叙述正确的是( )NH+4组卷:45引用:5难度:0.9 -
 4.有一化学平衡mA(g)+nB(g)⇌pC(g)+qD(g),如图表示的是A的转化率与压强、温度的关系.下列正确的是( )组卷:88引用:8难度:0.7
4.有一化学平衡mA(g)+nB(g)⇌pC(g)+qD(g),如图表示的是A的转化率与压强、温度的关系.下列正确的是( )组卷:88引用:8难度:0.7 -
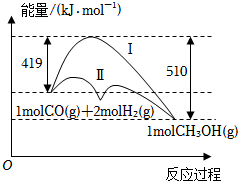 5.利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)⇌CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )组卷:35引用:1难度:0.6
5.利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)⇌CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )组卷:35引用:1难度:0.6 -
6.已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10是三种酸HNO2、HCN、HF的电离平衡常数,若已知这些酸可发生如下反应:①NaCN+HNO2=HCN+NaNO2 ②NaNO2+HF=HNO2+NaF,由此可判断下列叙述中不正确的是( )
组卷:26引用:3难度:0.7
二、非选择题:本题共4小题,共56分。
-
19.丙烯是重要的有机化工原料,丙烷脱氢是工业生产丙烯的重要途径,其化学方程式为C3H8(g)⇌C3H6(g)+H2(g) ΔH=+123kJ•mol-1回答下列相关问题:
(1)一定温度下,向1L的密闭容器中充入1molC3H8发生脱氢反应,经过10min达到平衡状态,测得平衡时气体压强是开始的1.5倍。
①0~10min丙烯的化学反应速率v(C3H6)=mol-1•L-1•min-1。
②下列情况能说明该反应达到平衡状态的是。
A.ΔH不变
B.C3H6与H2的物质的量之比保持不变
C.混合气体的总压强不变
D.c(C3H6)正=c(C3H6)逆
③欲提高丙烷转化率,采取的措施是(填字母标号)
A.降低温度
B.升高温度
C.加催化剂
D.及时分离出H2
④若在恒温、恒压的密闭容器中充入丙烷和氩气发生脱氢反应,起始n(氩气)/n(丙烷)越大,丙烷的平衡转化率越大,其原因是。
(2)一定温度下,向恒容密闭容器中充入1molC3H8,开始总压强为pkPa,平衡时总压发生变化(压强之比等于物质的量之比),C3H8的气体体积分数与反应时间的关系如图所示: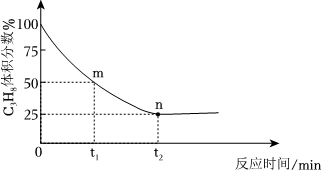
①此温度下该反应的平衡常数Kp=(用含字母p的代数式表示,Kp是用反应体系中气体物质的分压表示的平衡常数,平衡分压=总压×体积分数)
②已知该反应过程中,v正=k正p(C3H8),v逆=k逆p(C3H6)p(H2),其中k正、k逆为速率常数,只与温度有关,则图中n点处k逆:k正=。
(3)工业上,CO2与H2混合气体以一定的比例和一定流速分别通过填充有倠化剂Ⅰ、Ⅱ的反应器,CO2转化率与温度的关系如图。在催化剂Ⅱ作用下,温度高于T1时,CO2转化率下降的原因可能是。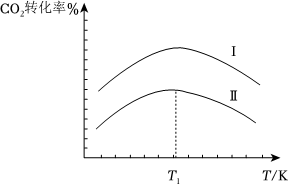 组卷:26引用:1难度:0.5
组卷:26引用:1难度:0.5 -
20.有下列物质:
Ⅰ.①石墨;②稀硫酸;③NH3;④氨水;⑤KHS;⑥NaHSO4;⑦CH3COOH;⑧HCl;⑨C2H5OH。
(1)属于非电解质的是。
(2)写出⑥在熔融状态下的电离方程式。
(3)向⑧溶液中加入醋酸钠晶体后,与足量的Zn粒反应,产生氢气的速率(填“变快”、“变慢”、“不变”);产生氢气的总量(填“增多”、“减少”、“不变”)。
Ⅱ.在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)⇌2NH3(g) ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示,请回答下列问题: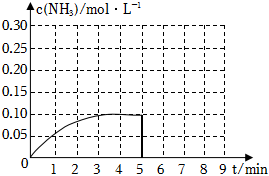
(4)该反应达到平衡时H2的转化率为。
(5)反应达到平衡后,第5min末,若保持其他条件不变,仅改变反应温度,则NH3的物质的量浓度不可能为。(填序号)。
a.0.20mol•L-1
b.0.12mol•L-1
c.0.10mol•L-1
d.0.08mol•L-1
(6)反应达到平衡后,第5min末,若保持其他条件不变,只把容器的体积缩小一半,平衡移动(填“向逆反应方向”、“向正反应方向”或“不”)。
(7)在第5min末将容器的体积缩小一半后,若在第8min末达到新的平衡(此时NH3的浓度约为0.25mol•L-1)请在图中画出第5min末到平衡时NH3浓度的变化曲线。组卷:6引用:1难度:0.5


