鲁科版(2019)选择性必修1《2.3 化学反应的速率》2023年同步练习卷(10)
发布:2024/8/17 5:0:1
一、选择题
-
1.已知:4NH3+5O2═4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系正确的是( )
组卷:443引用:20难度:0.9 -
2.在温度不变、恒容的容器中进行反应H2⇌2H△H>0,若反应物的浓度由0.1mol•L-1降到0.06mol•L-1需20s,那么由0.06mol•L-1降到0.036mol•L-1,所需反应时间应( )
组卷:109引用:12难度:0.9 -
3.100mL 2mol/L的盐酸与过量的锌片反应时,为减慢反应速率,又不影响生成的氢气的总量,可采用的方法是( )
组卷:84引用:3难度:0.7 -
4.反应 C(s)+H2O(g)⇌CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
①增加C的量
②将容器的体积缩小一半
③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积变大组卷:61引用:3难度:0.6 -
5.不同条件下,用O2氧化amol/L FeCl2溶液过程中所测的实验数据如图所示。下列分析或推测合理的是( )
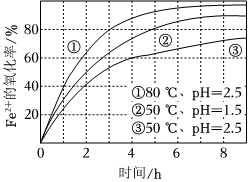 组卷:110引用:10难度:0.7
组卷:110引用:10难度:0.7
四、实验题
-
14.为了探究化学反应速率和化学反应限度的有关问题,某研究小组进行了以下实验:
Ⅰ.以H2O2的分解反应为研究对象,实验方案与数据记录如表,t表示收集a mL O2所需的时间:
(1)设计实验2和实验3的目的是研究序号 反应
温度/℃c(H2O2)/
mol•L-1V(H2O2)
/mLm(MnO2)
/gt/min 1 20 2 10 0 t1 2 20 2 10 0.1 t2 3 20 4 10 0.1 t3 4 40 2 10 0.1 t4 对化学反应速率的影响;
(2)为研究温度对化学反应速率的影响,可以将实验和实验作对比(填序号);
(3)将实验1和实验2作对比,t1t2(填“>”、“<”或“=”).
Ⅱ.以KI和FeCl3反应为例(2Fe3++2I-⇌2Fe2++I2)设计实验,探究此反应存在一定的限度.可选试剂:
①0.1mol•L-1KI溶液②0.1mol•L-1 FeCl3溶液③0.1mol•L-1 FeCl2溶液
④0.1mol•L-1盐酸⑤0.1mol•L-1KSCN溶液⑥CCl4
实验步骤:
(1)取5mL 0.1mol•L-1 KI溶液,再滴加几滴0.1mol•L-1 FeCl3溶液;
(2)充分反应后,将溶液分成三份;
(3)取其中一份,加试剂⑥,振荡,CCl4层显紫色,说明反应生成碘;
(4)另取一份,加试剂(填序号),现象,说明此反应存在一定的限度.
Ⅲ.N2O4可分解为NO2.在100mL密闭容器中投入0.01mol N2O4,利用现代化学实验技术跟踪测量c(NO2).c(NO2)随时间变化的数据记录如图所示: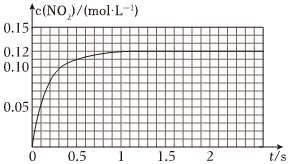
(1)反应容器中最后剩余的物质有,其中N2O4的物质的量为mol;
(2)c(NO2)随时间变化的曲线表明,实验测得的化学反应速率在逐渐减小,最后.(选填“变大”,“变小”或“不变”)组卷:18引用:2难度:0.3
五、解答题
-
 15.氮的氧化物是造成大气污染主要物质,研究氮氧化物间的相互转化及脱除对缓解环境污染具有重要意义。
15.氮的氧化物是造成大气污染主要物质,研究氮氧化物间的相互转化及脱除对缓解环境污染具有重要意义。
(1)CO还原NO的脱硝反应:2CO(g)+2NO(g)⇌2CO2(g)+N2(g)△H
已知:CO(g)+NO2(g)⇌CO2(g)+NO(g)△H1=-226kJ•mol-1
N2(g)+2O2(g)⇌2NO2(g)△H2=+68kJ•mol-1
N2(g)+O2(g)⇌2NO(g)△H3=+183kJ•mol-1
脱硝反应△H=,有利于提高NO平衡转化率的条件是、。(写出两条)
(2)已知2NO(g)+O2(g)⇌2NO2(g)的反应历程分两步:
第一步2NO(g)⇌N2O2(g)(快反应);
第二步N2O2(g)+O2(g)⇌2NO2(g)(慢反应)
下列关于反应2NO(g)+O2(g)⇌2NO2(g)的说法正确的是。(填序号)
A.压缩体积增大压强,正逆反应速率均一定增大
B.第一步反应的活化能小于第二步反应的活化能
C.第一步反应的速率决定总反应速率快慢
(3)某温度下,向体积为2L的恒容容器中通入2.00mol NO2,发生反应:2NO2(g)⇌N2O4(g)△H=57.0kJ•mol-1,已知:v正(NO2)=k1•c2(NO2),v逆(N2O4)=k2•c(N2O4),其中k1、k2为速率常数测得NO2的体积分数[α(NO2)]与反应时间(t)的关系如表。
则①平衡时,c(N2O4)=t/min 0 20 40 60 80 α(NO2) 1.0 0.75 0.52 0.50 0.50 。(计算结果保留两位小数)
②的数值为K1K2。
(4)以NH3为还原剂在脱硝装置中消除烟气中的氮氧化物。
主反应:4NH3(g)+4NO(g)═4N2(g)+6H2O(g)△H1=-1626.9kJ/mol-1
副反应:4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H2=-907.3kJ/mol-1
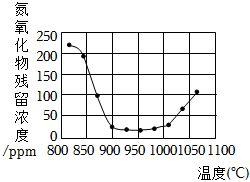
将烟气按一定的流速通过脱硝装置,测得出口NO的浓度与温度的关系如图,试分析脱硝的适宜温度是(填序号)。温度超过1000℃,NO浓度升高的原因是。
A.<850℃
B.900~1000℃
C.>1050℃组卷:33引用:2难度:0.5


