人教版(2019)选择性必修1《第1章 化学反应的热效应》2023年单元测试卷
发布:2024/8/16 15:0:1
一、选择题
-
1.下列图示变化为吸热反应的是( )
组卷:389引用:26难度:0.6 -
2.已知热化学方程式:2SO2(g)+O2(g)⇌2SO3(g)△H=-QkJ•mol-1(Q>0)。下列说法正确的是( )
组卷:27引用:2难度:0.7 -
3.苯燃烧热的热化学方程式为C6H6(l)+
O2(g)=6CO2(g)+3H2O(l)△H=-3260kJ•mol-1,设阿伏加德罗常数的值为NA,下列说法正确的是( )152组卷:73引用:3难度:0.9 -
4.下列热化学方程式的书写正确的是(已知:氢气、一氧化碳、乙醇、甲烷的标准燃烧热分别为:-285.8 kJ•mol-1、-283.0 kJ•mol-1、-1366.8 kJ•mol-1、-890.3 kJ•mol-1)( )
组卷:54引用:5难度:0.8 -
5.反应A+B→C(△H<0)分两步进行:①A+B=X(△H>0),②X→C(△H<0)。下列图象能正确表示该反应过程中的能量变化的是( )
组卷:48引用:5难度:0.7 -
6.下列有关热化学方程式的评价合理的是( )
实验事实 热化学方程式 评价 A 已知H+(aq)+OH-(aq)═H2O(l)
△H=-57.3 kJ•mol-1,将稀硫酸与稀氢氧化钡溶液混合H2SO4(aq)+Ba(OH)2(aq)
═BaSO4(s)+2H2O(l)
△H=-114.6 kJ•mol-1正确 B 醋酸与稀氢氧化钠溶液混合 CH3COOH(aq)+NaOH(aq)
═NaCl(aq)+H2O(l)
△H=-57.3kJ•mol-1不正确;因为醋酸状态为“aq”,而不是“l”. C 160 g SO3气体与适量水恰好完全反应生成H2SO4,放出热量260.6 kJ SO3(g)+H2O(l)═H2SO4(aq)
△H=-130.3 kJ•mol-1不正确;因为反应热为△H=-260.6kJ•mol-1 D 已知25℃、101 kPa下,120g石墨完全燃烧放出热量3935.1 kJ C(s)+O2(g)═CO2(g)
△H=-393.51 kJ•mol-1不正确;同素异形体要注名称:C(石墨) 组卷:208引用:10难度:0.7
五、解答题
-
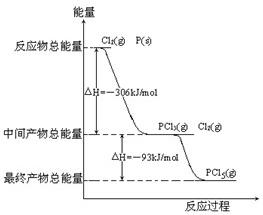 19.红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).
19.红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式.
(2)P和Cl2分两步反应生成1mol PCl5的△H1=,P和Cl2一步反应生成1mol PCl5的△H2△H1(填“>”、“<”或“=”).组卷:17引用:3难度:0.7 -
 20.锡、铅均是第ⅣA 族元素.在溶液中Pb2+很稳定而为Pb4+不稳定.
20.锡、铅均是第ⅣA 族元素.在溶液中Pb2+很稳定而为Pb4+不稳定.
(1)加热条件下用CO还原PbO可得到单质铅.已知:
①2Pb(s)+O2(g)=2PbO(s)△H=-438kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
则CO还原PbO的热化学方程式为.
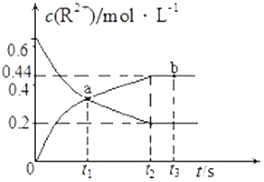
(2)硝酸铅与锡可发生置换反应:Pb2++Sn⇌Pb+Sn2+,常温下,反应过程中金属离子(R2+表示Pb2+、Sn2+)浓度随时间的变化情况如图所示:
①t1、t2时刻生成Sn2+速率较大的是.
②若将500ml 1.2mol/LPb(NO3)2与2.4mol/LSn(NO3)2等体积混合后,再向溶液中加入0.2molPb、0.2molSn,此时v(正)v(逆)(填“>”、“<”).
(3)消除废水中Pb2+造成污染的方法有多种,其中之一是将其转化为沉淀,已知常温下几种铅的难溶化合物的Ksp:Ksp[Pb(OH)2]=1.2×10-16,Ksp(PbS)=8×10-28,从更有利于除去污水中Pb2+的角度看,处理效果最差的是将Pb2+转化为沉淀.若用FeS将Pb2+转化为PbS,则相应转化反应的平衡常数K=(已知Ksp(FeS)=6×10-18).
(4)铅元素在生活中常用做铅蓄电池,请写出铅蓄电池充电时的总反应方程式:.组卷:35引用:2难度:0.3


