2023-2024学年北京市高三(上)入学定位化学试卷
发布:2024/8/17 5:0:1
一、选择题:每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
-
1.下列材料的主要成分属于有机化合物的是( )
组卷:52引用:3难度:0.9 -
2.下列有关物质的性质与用途的叙述中,对应关系正确的是( )
组卷:6引用:1难度:0.7 -
3.下列说法正确的是( )
组卷:70引用:3难度:0.7 -
4.用化学用语表示NH3+HCl═NH4Cl中的相关微粒,其中正确的是( )
组卷:58引用:5难度:0.8 -
5.稀溶液中,单位体积内溶质的分子或离子数目越多,该溶液的沸点越高。下列浓度均为0.01mol/L的溶液的沸点由高到低依次是( )
①蔗糖溶液
②K2SO4溶液
③NaCl溶液
④醋酸溶液组卷:31引用:1难度:0.7 -
6.下列反应的原理用离子方程式表示正确的是( )
组卷:10引用:1难度:0.7
二、非选择题:本部分共5题,共58分。
-
18.软锰矿在生产中有广泛的应用。

(1)过程Ⅰ:酸浸
①用稀H2SO4溶液处理软锰矿后,溶液中含有Fe3+,矿粉颗粒表面附着有黄色固体硫。上述过程中的主要反应为(将方程式补充完整):2FeS2+MnO2+=++4S+。
②硫附着在矿粉颗粒表面不利于酸浸进行,加入H2O2可以提高锰元素的浸出率。
结合化学方程式说明H2O2的作用原理:(写出两条)
i;
ii。
(2)过程Ⅱ:
①使用过量MnCO3固体可以去除酸浸后滤液中的Fe3+。选用MnCO3的理由是。
②制备Mn3O4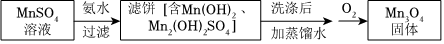
如图表示通入O2时pH随时间的变化: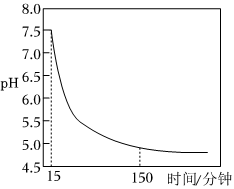
0~15分钟,pH几乎不变;15~150分钟,pH明显降低。结合方程式解释原因:。组卷:8引用:2难度:0.5 -
19.探究pH对FeSO4溶液的配制和保存的影响。
Ⅰ.FeSO4溶液的配制
将0.28g(1×10-3mol)FeSO4⋅7H2O分别溶于10mL蒸馏水或10mL稀硫酸,现象如表:
(1)用离子方程式表示①中溶液显酸性的主要原因编号 溶剂 溶液性状 ① 蒸馏水 浅黄色澄清溶液 pH=3.8;滴加1mol/LKSCN溶液无明显变化 ② 0.01mol/LH2SO4 无色澄清溶液 pH=1.8;滴加1mol/LKSCN溶液微微变红 ③ 2mol/LH2SO4 无色澄清溶液 滴加1mol/LKSCN溶液微微变红 。
(2)甲同学认为①溶液中一定有+3价铁。他用激光笔照射“溶液”,观察到光路;向含有KSCN的①溶液中滴入试剂a,溶液变红,说明其推断正确。试剂a是。
Ⅱ.FeSO4溶液的保存
将实验Ⅰ中配制的三份溶液分别在空气中放置24小时后,记录如表。
(3)①中的浑浊主要是FeOOH,用离子方程式表示其生成过程编号 溶液性状 ① 橙色浑浊 用H2SO4酸化后,浊液变澄清,再滴加1mol/LKSCN溶液后变深红 ② 无色溶液 滴加1mol/L的KSCN溶液后显浅红色 ③ 无色溶液 滴加1mol/L的KSCN溶液后显红色,颜色比②略深 。
(4)该实验的初步结论:保存FeSO4溶液的最佳pH是。
(5)进一步探究pH对FeSO4变质影响的原因。用如图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后: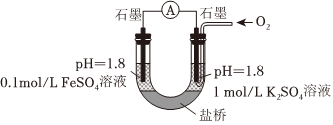
i.向左池滴加浓硫酸至c(H2SO4)接近2mol/L,电流没有明显变化;
ii.向右池滴加等量浓硫酸,电流明显增大。
已知:电流增大表明化学反应速率加快,在该实验条件下与物质的氧化性(还原性)增强有关。
a.结合电极反应式分析ii中电流增大的原因。
b.依据实验i和ii推断:③比②中FeSO4更易变质的原因是。
c.按上述原理进行实验,证实①中FeSO4更易变质的主要原因是Fe2+的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,。组卷:10引用:1难度:0.5


