2023年江苏省镇江市市区中考化学二模试卷
发布:2024/6/19 8:0:9
一、选择题(本题包括20小题,每小题2分,共40分,每小题只有一个选项符合题意。)
-
1.下列属于纯净物的是( )
组卷:45引用:2难度:0.5 -
2.下列现象主要是由化学变化引起的是( )
组卷:51引用:2难度:0.7 -
3.下列物质的用途主要与化学性质有关的是( )
组卷:71引用:2难度:0.5 -
4.下列做法正确的是( )
组卷:15引用:2难度:0.5 -
5.下列归类正确的是( )
选项 归类 内容 A 合成材料 涤纶、聚乙烯、合成橡胶 B 可燃气体 氢气、氧气、一氧化碳 C 常见溶液 碘酒、液氮、石灰水 D 清洁能源 煤炭、风能、太阳能 组卷:30引用:2难度:0.6 -
6.实验室制备CO2,并测定CO2溶于水后溶液的pH,下列做法正确的是( )
组卷:33引用:2难度:0.6 -
7.下列实验方法正确的是( )
组卷:13引用:3难度:0.7 -
8.下列排序正确的是( )
组卷:84引用:2难度:0.5 -
9.下列指定反应的化学方程式正确的是( )
组卷:41引用:2难度:0.7 -
10.如图是甲转化为戊的微观过程,下列说法不正确的是( )
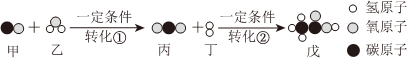 组卷:22引用:2难度:0.5
组卷:22引用:2难度:0.5
第Ⅱ卷(非选择题共60分)
-
29.现有一包白色固体,可能含有K2CO3、NaCl、(NH4)2SO4、NaOH、Ba(OH)2中的一种或几种。现做如下实验:
(1)取适量固体与熟石灰研磨有氨味,则原固体中一定含有。
(2)另取适量固体溶于足量水,得白色固体A和无色滤液B,则原固体一定含有。
(3)取少量固体A,加入足量稀HNO3,固体部分溶解,写出固体溶解的化学方程式。
(4)取少量滤液B,滴加无色酚酞溶液,呈红色,则原固体中(选填“一定”或“不一定”)含有NaOH。
(5)另取少量滤液B先滴入足量稀硝酸,再滴加足量溶液,静置后再滴加AgNO3溶液,出现白色沉淀,则原固体还含有NaCl。组卷:87引用:3难度:0.5 -
30.从古至今,铁及其化合物在生产生活中发挥着重要作用。
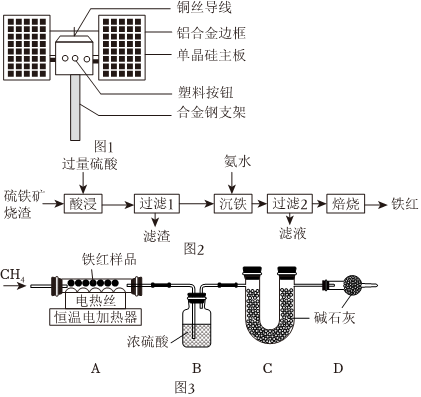
一、铁材料的认识
(1)钢铁是目前使用较广泛的金属。如图1是某太阳能电池示意图,其中不涉及到的材料是(选填字母)。
a.无机材料
b.合成材料
c.复合材料
(2)图中支架采用合金钢,相比于纯铁,它的硬度更(选填“大”或“小”)。
(3)《天工开物》记载的“炒钢”是靠鼓风并不断搅拌熔化的生铁使其成钢。“炒钢”是为了降低生铁中元素的含量。
(4)铁制品使用过程中容易生锈,实际上是铁与空气中的发生化学反应的过程。铁制品表面的铁锈,可加入稀盐酸除去,其原理是(用化学方程式表示)。
二、铁红(Fe2O3)的制备
工业上用硫铁矿烧渣(含有Fe2O3、FeO和SiO2等)制备铁红的步骤如图2所示。
(5)酸浸前,将烧渣粉碎的目的是。
(6)酸浸时,硫酸不能过量太多,一是节约硫酸,二是。
(7)“沉铁”过程温度不宜过高,主要原因是。
(8)“沉铁”后过滤,滤渣中含有FeOOH,将其焙烧后可得到铁红,写出焙烧时发生反应的化学方程式。
三、还原性铁粉的制备
上述流程制备的铁红混有少量FeOOH,实验小组取48.9g该铁红样品置于装置A中,通入CH4后加热制备还原性铁粉,不同温度下测得装置B和C的质量变化如表所示。
【资料】如图3所示。FeOOH在350℃时完全分解。加热到500℃以上,Fe2O3和CH4开始反应,生成铁的其他氧化物、CO2和H2O。温度高于700℃,生成Fe。
(9)装配好实验装置后,先要温度℃ 装置B/g 装置C/g 室温 200.0 200.0 350 200.9 200 600 m 201.1 650 202.7 202.2 。
(10)停止加热后还要持续通入一段时间CH4,目的是防止倒吸和。
(11)表中m=。
(12)加热到600℃时,装置A中剩余固体的化学式为。
(13)650℃时,A中剩余固体为FeO和Fe3O4的混合物,写出装置A中固体由Fe2O3加热到650℃时发生反应的总化学方程式。组卷:122引用:2难度:0.5


