人教版(2019)必修第一册《4.2.2 元素周期表和元素周期律的应用》2023年同步练习卷(1)
发布:2024/7/18 8:0:9
一、选择题
-
1.已知某元素的最高化合价为+7价,下列说法中正确的是( )
组卷:110引用:10难度:0.9 -
2.某主族元素R的最高正价与最低负化合价的代数和为4,由此可以判断( )
组卷:23引用:5难度:0.7 -
3.X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示。下列说法错误的是( )
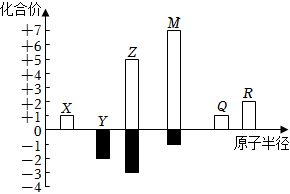 组卷:225引用:25难度:0.7
组卷:225引用:25难度:0.7 -
4.应用元素周期律判断下列语句,其中正确的组合是( )
①碱金属(即ⅠA族)单质的熔点随原子序数的增大而降低
②砹(At)是第ⅦA族元素,其氢化物的稳定性大于HCl
③硒(Se)的最高价氧化物对应水化物的酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
⑥第三周期金属元素的最高价氧化物对应的水化物,其碱性随原子序数的增大而减弱组卷:27引用:3难度:0.5 -
5.下列各组中的性质比较,正确的是( )
①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
③还原性:F->Cl->Br-
④稳定性:HCl>H2S>PH3
⑤熔沸点:HI>HBr>HCl>HF.组卷:115引用:5难度:0.9
二、填空题
-
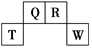 16.短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期数与主族序数相等。
16.短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期数与主族序数相等。
请回答下列问题:
(1)W在周期表中的位置是,Q、R、T三种元素原子半径由大到小的顺序为。(用元素符号表示),QO2的电子式为,R的最高价氧化物的化学式。
(2)T单质与NaOH 溶液反应的离子方程式为。组卷:193引用:2难度:0.6
三、解答题
-
17.表是元素周期表的一部分,针对表中①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在①~⑦元素中,原子半径最小的是主族
周期ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 二 ① ② 三 ③ ④ ⑤ ⑥ ⑦ ⑧ 四 ⑨ ⑩ ;原子半径最大的是,其离子结构示意图为
(2)①~⑩元素的最高价氧化物对就的水化物中酸性最强的是,碱性最强的是;
(3)按要求写出下列两种物质的电子式:①的氢化物;⑨的最高价氧化物对应的水化物;
(4)在⑦与⑩的单质中,化学性质较活泼的是,可用1个化学反应说明该事实(写出反应的化学方程式):.组卷:7引用:3难度:0.3


