2022-2023学年天津市新四区示范校高一(下)期末化学试卷
发布:2024/6/6 8:0:9
一、单选题(本大题共12小题,共60分)
-
1.热还原法冶炼金属的反应一定是( )
组卷:82引用:13难度:0.7 -
2.下列电池工作时,O2在正极放电的是( )
组卷:57引用:7难度:0.5 -
3.下列有机反应属于酯化反应的是( )
组卷:162引用:5难度:0.8 -
4.下列关于有机化合物的说法正确的是( )
组卷:81引用:4难度:0.9 -
5.下列有关四个常用电化学装置的叙述中,正确的是( )
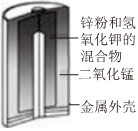
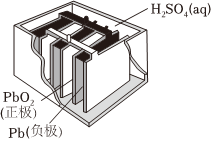
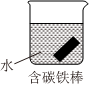
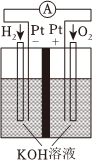
图Ⅰ碱性锌锰电池 图Ⅱ铅蓄电池 图Ⅲ 图Ⅳ氢氧燃料电池 组卷:53引用:2难度:0.7
二、简答题(本大题共4小题,共40分)
-
15.生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水的。
(2)工业上用乙烯与水反应可制得乙醇,该反应的反应类型是。
(3)下列属于乙醇的同系物的是,属于乙醇的同分异构体的是。(填编号)
A.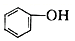
B.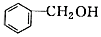
C.乙醚(CH3CH2OCH2CH3)
D.甲醇
E.CH3-O-CH3
F.HO-CH2CH2-OH
(4)乙醇能够发生氧化反应:
①46g乙醇完全燃烧消耗mol氧气。
②乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为。组卷:81引用:3难度:0.5 -
 16.Ⅰ.氮是地球上含量丰富的一种元素,氮及其化合物在工、农业生产、生活中有着重要作用。
16.Ⅰ.氮是地球上含量丰富的一种元素,氮及其化合物在工、农业生产、生活中有着重要作用。
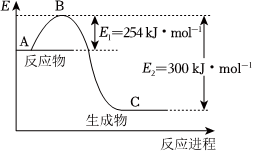
(1)如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:。
(2)若已知下列数据:
试根据表中及图中数据计算N-H的键能化学键 H-H N≡N 键能/kJ•mol-1 435 943 kJ•mol-1。
(3)用NH3催化还原NOX还可以消除氮氧化物的污染。例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H1=nkJ•mol-1
N2(g)+O2(g)=2NO(g)△H2=mkJ/mol
若1molNH3还原NO至N2,则该反应过程中的反应热△H3=kJ/mol(用含a、b的式子表示)。
Ⅱ.氨的合成是最重要的化工生产之一。已知:N2+3H2⇌2NH3,在3个体积均为2L的密闭容器中,在相同的温度下,使用相同的催化剂合成氨,实验测得反应在起始、达到平衡时的有关数据如下表所示:
试回答:容器 甲 乙 丙 反应物投入量 3molH2、2molN2 6molH2、4molN2 2molNH3 达平衡时间(min) 5 8 N2浓度(mol/L) C1 1.5 NH3的体积分数 W1 W3 混合气体密度(g/L) ρ1 ρ2
(4)下列各项能说明该反应已达到平衡状态的是(填写序号字母)。
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.3v(N2)正=v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(5)分析上表数据,下列关系正确的是(填写序号字母)。
A.2c1<1.5mol•L-1
B.2ρ1=ρ2
C.w3=w1
D.K甲=K乙=K丙
(6)容器乙中反应从开始到达平衡平均速率为v(H2)=mol/(L•min)。
Ⅲ.直接供氨式碱性燃料电池的电池反应式是4NH3+3O2=2N2+6H2O,电解质溶液一般使用KOH溶液。
(7)负极电极反应式是。组卷:70引用:3难度:0.7


