2022-2023学年北京师大附属实验中学高一(下)期中化学试卷
发布:2024/9/20 6:0:10
一、(选择题共45分)
-
1.下列过程属于人工固氮的是( )
组卷:72引用:6难度:0.9 -
2.常温下,下列溶液可用铁质容器盛装的是( )
组卷:263引用:14难度:0.5 -
3.下列金属,在工业上常用电解法冶炼的是( )
组卷:23引用:2难度:0.8 -
4.下列物质中属于含有共价键的强电解质的是( )
组卷:89引用:2难度:0.8 -
5.取一支试管,收集半试管CH4和半试管Cl2,在光照下得到的取代产物是( )
①CH3Cl
②CH2Cl2
③CHCl3
④CCl4组卷:515引用:8难度:0.6 -
6.下列离子半径最小的是( )
组卷:119引用:2难度:0.8 -
7.某有机物的结构简式为CH2=CHCH2CH2OH,不能与该有机物发生反应的物质有( )
组卷:34引用:1难度:0.8
二、填空题(共55分)
-
20.锗Ge及其化合物应用于航空航天测控、光纤通讯等领域、一种提纯二氧化锗粗品(主要含GeO2、As2O3)的工艺如图:
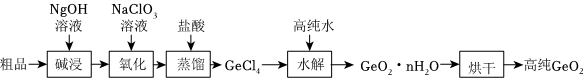
已知:ⅰ.Ge位于第四周期ⅣA族,GeO2为两性氧化物,GeCl4沸点低.
ⅱ.As位于第四周期ⅤA族,As2O3为两性氧化物,As2Cl3沸点低.
(1)写出“碱浸”过程中GeO2发生反应的离子方程式.
(2)“氧化”过程是将Na3AsO3氧化为As的最高价的化合物.
①理论上消耗Na3AsO3与NaClO3的物质的量之比为.
②如果没有“氧化”过程,产生的影响可能是.
(3)“水解”过程得到沉淀GeO2⋅nH3O,过滤,滤液经过处理后可用于过程,实现物质循环利用.组卷:34引用:1难度:0.5 -
21.某小组同学制备碘酸盐(
)并探究其性质.IO-3
资料:①I2可与NaOH溶液反应生成和I-.IO-3
②碘酸钙[Ca(IO3)2]为难溶于水、能溶于硝酸的白色固体.
③X2的氧化性,X-的还原性与溶液的酸碱性无关:与氧化性随溶液酸性增强而增强(X为Cl、Br或I).IO-3
实验装置如图(加热与夹持装置略):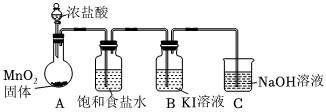
步骤:
Ⅰ.打开A中分液漏斗活塞,加热固底烧瓶;一段时间后,B中溶液由无色变为棕黄色.
Ⅱ.将B中棕黄色溶液倒入烧杯中,再加入NaOH溶液,烧杯中溶液由棕黄色变为无色.
(1)A装置发生的化学方程式为.
(2)C装置发生的离子方程式为.
(3)取少量步骤Ⅱ后所得无色溶液,加入过量盐酸和CCl4,振荡后静置,溶液分层,上层呈浅黄色,下层呈紫色.甲同学得出结论:在酸性条件下可以氧化I-为I2.IO-3
①乙同学认为上述结论不合理,可能原因如下:
原因一:空气中O2在酸性条件下将溶液中的I-氧化,离子方程式为.
原因二:(填化学式)在酸性条件下将溶液中的I-氧化.
②为了进一步证明在酸性条件下可氧化I-为I2,完成如下实验:IO-3
ⅰ.另取与(3)等量的步骤Ⅱ后所得无色溶液,加入稍过量CaCl2固体,振荡,充分反应后过滤得到无色溶液X和沉淀Y.
ⅱ.向无色溶液X,加入与(3)等量的盐酸和CCl4,振荡后静置,溶液分层,上、下层均几乎无色.
ⅲ.取少量洗涤后的沉淀Y加入稀HNO3,固体溶解,继续加入少量KI溶液,溶液呈黄色.
ⅳ.……
a.由实验ⅰ、ⅱ得出结论:.
b.由实验ⅲ和ⅳ得出结论:在酸性条件下可以氧化I-为I2.补全实验ⅳ的操作和现象IO-3.
(4)根据实验ⅲ得出:氧化性I2(填“>”或“<”),而实验ⅰ表明I2和IO-3的氧化性强弱关系相反,原因是IO-3.
(5)查阅资料发现,与相应的X-(X=Cl,Br)均有类似上述反应.浓度相同时,氧化性XO-3≈ClO-3,但浓度均为0.1mol/L的BrO-3和Cl-开始发生反应时的pH为1,而浓度均为0.1mol/L的ClO-3和Br-开始发生反应的pH为5.试从原子结构的角度解释两个反应开始发生时pH不同的原因BrO-3.组卷:102引用:5难度:0.4


