当前位置:
章节挑题
请展开查看知识点列表
>
更多>>
 已完结
已完结
|
热点预测
中考复习
热搜题专练
浏览次数:270
更新:2025年04月27日
|
 已完结
已完结
|
热点预测
高考复习
新题抢练
浏览次数:322
更新:2025年04月25日
|
251.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图所示。
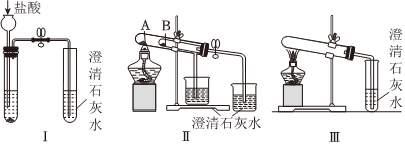
(1)只根据图Ⅰ所示实验,不能够达到实验目的原因是。
(2)图Ⅱ、Ⅲ所示实验均能鉴别这两种物质,其反应的化学方程式为。
(3)若用实验Ⅱ验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体最好是(填化学式)。发布:2024/5/23 20:38:36组卷:101引用:4难度:0.5252.关于Na2CO3和NaHCO3比较中,下列说法不正确的是( )
发布:2024/5/23 20:38:36组卷:176引用:14难度:0.9253.下列反应中的氨与反应4NH3+5O2→4NO+6H2O中的氨作用相同的是( )
发布:2024/5/23 20:38:36组卷:1463引用:20难度:0.7254.过氧化氢(H2O2,氧显-1价)俗名双氧水,医疗上利用它杀菌消毒的作用来清洗伤口。

根据下列反应回答问题:
A.Ag2O+H2O2═2Ag+O2↑+H2O
B.2H2O2═2H2O+O2↑
C.3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2分别表现性质。
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序。
(3)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:
O2、MnO4-、H2O、Mn2+、H2O2、H+.已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式为。发布:2024/5/23 20:38:36组卷:44引用:2难度:0.7255.铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的HCl和NaOH的物质的量之比是( )
发布:2024/5/23 20:38:36组卷:107引用:10难度:0.9256.“纳米材料”是粒子直径为几纳米至几十纳米的材料,纳米碳就是其中一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质 ①是溶液 ②是胶体 ③能产生丁达尔效应 ④不能透过滤纸 ⑤能透过滤纸 ⑥静置后会析出黑色沉淀( )
发布:2024/5/23 20:38:36组卷:77引用:3难度:0.9257.钛和钛合金是21世纪的重要金属材料。它们具有优良的性能,如熔点高、密度小、可塑性好、机械性能好、抗腐蚀能力强,钛合金与人体有很好的“相容性”。根据它们的主要性能判断,下列不合实际的用途是( )
发布:2024/5/23 20:38:36组卷:17引用:2难度:0.6258.将 1.5g 两种金属的混合物粉末与足量的盐酸反应,反应完全后,得到标准状况下的氢气 1.12L.则这 两种金属可能是( )
发布:2024/5/23 20:38:36组卷:165引用:4难度:0.5259.下列溶液中c(Cl-)与150mL 1mol/L NaCl溶液中c(Cl-)相等的是( )
发布:2024/5/23 20:38:36组卷:80引用:6难度:0.7 260.KOH是我国古代纺织业常用作漂洗的洗涤剂。古代制取KOH的流程如图,流程中没有涉及的化学反应类型是( )发布:2024/5/23 20:38:36组卷:32引用:2难度:0.8
260.KOH是我国古代纺织业常用作漂洗的洗涤剂。古代制取KOH的流程如图,流程中没有涉及的化学反应类型是( )发布:2024/5/23 20:38:36组卷:32引用:2难度:0.8



