当前位置:
章节挑题
请展开查看知识点列表
>
更多>>
 已完结
已完结
|
期末复习
典型试卷
考前必刷
浏览次数:1035
更新:2025年06月03日
|
 已完结
已完结
|
热点预测
高考复习
难题抢练
浏览次数:1229
更新:2025年05月26日
|
981.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理如下:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+O2(g)═CO2(g)+2H2(g)△H=-192.9kJ/mol12
下列说法正确的是( )发布:2024/4/20 14:35:0组卷:17引用:5难度:0.7982.在1.5L的密闭容器中通入2molN2和3molH2的混合气体,在一定条件下发生反应.达到平衡时,容器内压强为反应开始时的0.8倍,则该反应的化学平衡常数为( )
发布:2024/4/20 14:35:0组卷:20引用:7难度:0.9983.为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得,1g乙醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出29.7kJ的热量,试写出表示乙醇燃烧热的热化学方程式:。
(2)已知反应CH3-CH3(g)═CH2=CH2(g)+H2(g),有关化学键的键能如下:
通过计算得出该反应的反应热为化学键 C-H C=C C-C H-H 键能/(kJ•mol-1) 414.4 615.3 347.3 435.3 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(石墨,s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2 599kJ•mol-1
根据盖斯定律,计算298K时由C(石墨,s)与H2(g)生成1mol C2H2(g)反应的焓变:
△H=。发布:2024/4/20 14:35:0组卷:17引用:3难度:0.6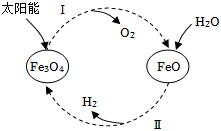 984.已知:2H2O(l)═2H2(g)+O2(g)△H=+571.6kJ•mol-1。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的图示与过程如下:
984.已知:2H2O(l)═2H2(g)+O2(g)△H=+571.6kJ•mol-1。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的图示与过程如下:
过程Ⅰ:……
过程Ⅱ:3FeO(s)+H2O(l)═H2(g)+Fe3O4(s)△H=+129.2kJ•mol-1
下列说法正确的是( )发布:2024/4/20 14:35:0组卷:37引用:3难度:0.7985.下列实验误差分析错误的是( )
发布:2024/4/20 14:35:0组卷:34引用:6难度:0.7986.通过以下反应可获得新型能源二甲醚(CH3OCH3 )。下列说法不正确的是 ( )
①C(s)+H2O(g)═CO(g)+H2 (g)△H1=a kJ•mol-1
②CO(g)+H2O(g)═CO2(g)+H2 (g)△H2=b kJ•mol-1
③CO2 (g)+3H2 (g)═CH3OH(g)+H2O(g)△H3=c kJ•mol-1
④2CH3OH(g)═CH3OCH3 (g)+H2O(g)△H4=d kJ•mol-1。发布:2024/4/20 14:35:0组卷:100引用:19难度:0.6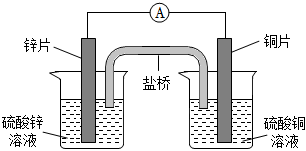 987.关于如图所示的原电池,下列说法正确的是( )发布:2024/4/20 14:35:0组卷:110引用:7难度:0.7
987.关于如图所示的原电池,下列说法正确的是( )发布:2024/4/20 14:35:0组卷:110引用:7难度:0.7



