当前位置:
章节挑题
请展开查看知识点列表
>
更多>>
 已完结
已完结
|
热点预测
中考复习
热搜题专练
浏览次数:222
更新:2025年04月27日
|
 已完结
已完结
|
热点预测
高考复习
新题抢练
浏览次数:306
更新:2025年04月25日
|
101.怎样理解Cl2、Br2、I2的键能依次下降,键长依次增大?
发布:2024/5/23 20:38:36组卷:23引用:2难度:0.8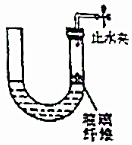 102.某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),化学反应方程式如下:
102.某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),化学反应方程式如下:
①2Na2O2+2CO2═2Na2CO3+O2
②2Na2O2+2H2O═4NaOH+O2↑
(1)反应①中含极性键的非极性分子的电子式为。反应②中含极性键的离子化合物的电子式为。
(2)常温下,CO2为气体但CS2却为液体,请用物质结构知识说明原因。
(3)实验中,用大理石、稀盐酸制取所需CO2,装置如图。简述检验气密性的操作方法,将气体通过Na2O2前必须除去的杂质是,该除杂剂是。
(4)确认实验中生成O2的操作方法是。发布:2024/5/23 20:38:36组卷:84引用:3难度:0.6103.a、b、c、d为四种由短周期元素组成的物质,它们的组成微粒(化学式)中都含有14个电子,且四种物质中均只含共价键。试回答下列问题:
(1)a是单质,可用作半导体材料,则构成a物质的原子的核外电子排布式为。
(2)b是双核化合物,常温下为无色无味的气体,则b的化学式为。
(3)c是双核单质,其电子式为,c分子中所含共价键类型为(填“极性键”或“非极性键”)
(4)d是四核化合物,其结构式为,1个d分子中含有个σ键,个π键,其中σ键的强度(填“>”“<“或“=“)π键,原因是。发布:2024/5/23 20:38:36组卷:106引用:7难度:0.5104.X、Y、D、E、M、N是原子序数依次增大的前四周期元素,其中X是周期表中原子半径最小的元素,Y元素基态原子的三个能级上电子数目相同,E是地壳中含量最多的元素,M是制常见不锈钢材料的第一主要合金元素,其基态原子核外的未成对电子数在同周期元素中最多,N是目前用量最大的金属元素。
(1)N元素在周期表中的位置是,M的基态原子的价层电子排布图为。
(2)Y、D、E三种元素的电负性从大到小的排列顺序为,第一电离能从大到小的排列顺序为。(均用元素符号表示)。
(3)由X、D两种元素按原子个数比为2:1组成的化合物,其中心原子的杂化方式为,该化合物属于分子(填“极性”或“非极性”)。
(4)金属镍粉在化合物YE气流中轻微加热,生成无色挥发性液态Ni(YE)4,呈四面体构型。423K时,Ni(YE)4分解为Ni和YE,从而制得高纯度的Ni粉。试推测:该液态物质易溶于下列中(填字母)。
A.水 B.硫酸镍溶液 C.苯 D.四氯化碳
(5)某盐中含离子,是一种水处理剂,加入稀硫酸后快速生成黄色溶液并释放出一种无色无味的气体,请写出该反应的离子方程式NE2-4。发布:2024/5/23 20:38:36组卷:21引用:2难度:0.6 105.元素X、Y、Z在周期表中的相对位置如图所示,已知Y元素原子的价电子排布为ns(n-1)np(n+1),则下列说法不正确的是( )发布:2024/5/23 20:38:36组卷:8引用:3难度:0.7
105.元素X、Y、Z在周期表中的相对位置如图所示,已知Y元素原子的价电子排布为ns(n-1)np(n+1),则下列说法不正确的是( )发布:2024/5/23 20:38:36组卷:8引用:3难度:0.7106.下列原子中未成对电子(单独占据1个原子轨道的电子)数为2的是( )
发布:2024/5/23 20:38:36组卷:31引用:2难度:0.9107.某学生在做同一主族元素性质的递变规律的实验时,自己设计了一套实验方案,并记录了有关实验现象。现在请你帮助该学生整理并完成实验报告。
(1)实验目的:探究同一主族元素性质的递变规律。
(2)实验用品
仪器:试管、胶头滴管。
药品:新制的氯水、新制的溴水、溴化钠溶液、碘化钠溶液、四氯化碳。
(3)实验内容(在表中横线处填写相关内容):
(4)实验结论:序号 实验方案 实验现象 ① 向盛有少量溴化钠溶液的试管中滴加少量新制的氯水,振荡,再加入少量四氯化碳,振荡后静置 液体分为两层,下层呈 色② 向盛有少量碘化钠溶液的试管中滴加少量新制的溴水,振荡,再加入少量四氯化碳,振荡后静置 液体分为两层,下层呈 色。
(5)问题和讨论:
①上述两个实验中发生反应的离子方程式分别为、。
②请用本章所学内容简单说明得出上述结论的原因。发布:2024/5/23 20:38:36组卷:8引用:2难度:0.6108.一个价电子构型为2s22p5的元素,下列有关它的描述正确的有( )
发布:2024/5/23 20:38:36组卷:45引用:2难度:0.8109.PH3是一种无色剧毒气体,其分子结构和NH3相似,但P-H的键能比N-H的键能小。下列判断错误的是( )
发布:2024/5/23 20:38:36组卷:4引用:2难度:0.7110.第四周期的 Cr、Fe、Co、Ni、Cu、Zn 等许多金属能形成配合物。
(1)NH3是一种很好的配体,氨气分子是(填“极性”或“非极性”)分子,NH3的沸点(填“高于”“等于”或“低于”)AsH3。
(2)科学家通过 X 射线测得胆矾的结构示意图可简单表示如图:
图中虚线表示的作用力为。
(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4•H2O晶体。
在Cu(NH3)4SO4•H2O晶体中,含有的原子团或分子有:[Cu(NH3)4]2+、NH3、SO42-、H2O,其中[Cu(NH3)4]2+为平面正方形结构,则 VSEPR模型为四面体结构的原子团或分子是,其中心原子的杂化轨道类型是。
(4)金属镍粉在 CO 气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型。Ni(CO)4易溶于(填编号)。
a、水 b、四氯化碳 c、苯 d、硫酸镍溶液发布:2024/5/23 20:38:36组卷:58引用:5难度:0.6



