2022-2023学年湖北省武汉市常青联合体高二(上)期末化学试卷
发布:2024/5/8 8:0:8
一、选择题(本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合要求的)
-
1.科学家的发明与创造推动了人类文明的进程,下列有关说法中不正确的是( )
组卷:16引用:3难度:0.6 -
2.下列化学用语不正确的是( )
组卷:49引用:2难度:0.8 -
3.化学与生产生活密切相关。下列叙述错误的是( )
组卷:20引用:5难度:0.7 -
4.反应A(g)+3B(g)⇌2C(g)+2D(g)在四种不同情况下的反应速率分别为①v(A)=0.45mol/(L•min);②v(B)=0.6mol/(L•s);③v(C)=0.4mol/(L•s);④v(D)=0.45mol•L-1•s-1,该反应进行的快慢顺序为( )
组卷:177引用:8难度:0.7 -
5.为了除去MgCl2溶液中的Fe3+,可在加热并搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量盐酸,这种试剂是( )
组卷:27引用:2难度:0.6 -
6.常温下,下列各组离子在指定溶液中能大量共存的是( )
组卷:33引用:3难度:0.7
二、非选择题(本题共4题,共55分)
-
18.工业上利用软锰矿(主要成分为MnO2,含有少量Al2O3、Fe2O3、MgO、SiO2等杂质)冶炼金属锰的流程如图所示:
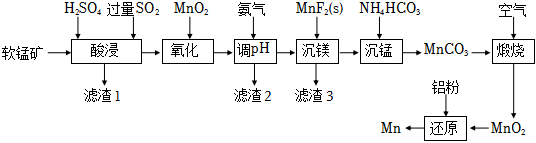
已知部分难溶物的溶度积常数见下表:
回答下列问题:难溶物 Mn(OH)2 MnF2 MgF2 溶度积(Ksp) 2.0×10-13 5.6×10-3 7.0×10-11
(1)“酸浸“步骤中被还原的物质有,该步骤中MnO2参与反应的离子方程式为。
(2)“滤渣2“的主要成分是,已知“氧化“后溶液中(Mn2+)=0.2mol•L-1,若调pH至6,则是否有Mn(OH)2析出,列式计算:。
(3)写出“沉镁“步骤的离子方程式:,该反应的平衡常数值为。
(4)“沉锰”时,若温度过高会产生含锰元素的副产物(写化学式);“沉锰“后的母液加入碱液,再加热处理可返回(填步骤名称)步骤循环利用。组卷:12引用:1难度:0.5 -
19.以NO2为主要成分的雾霾的综合治理是当前重要的研究课题。
Ⅰ.汽车尾气中的NO(g)和CO(g)在一定条件下可发生反应生成无毒的N2和CO2。
(1)已知:①N2(g)+O2(g)=2NO(g)ΔH1=+180.5kJ•mol-1
②CO的燃烧热 ΔH2=-283.0kJ•mol-1
则反应③2NO(g)+2CO(g)⇌N2(g)+2CO2 (g)ΔH3=。
(2)某研究小组在三个容积为5L的恒容密闭容器中,分别充入0.4molNO和0.4molCO,发生反应③。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示: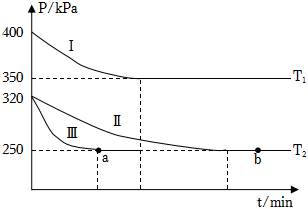
①温度:T1T2(填“<”“=”或“>”)。
②CO的平衡转化率:ⅠⅡⅢ(填“<”“=”或“>“)。
③反应速率:a点的v逆b点的v正(填“<”“=”或“>”)。
Ⅱ.N2O是一种强温室气体,且易形成颗粒性污染物,研究N2O的分解反应2N2O=2N2+O2对环境保护有重要意义。
(3)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)=2I(g)快速平衡,平衡常数为K
第二步:I(g)+N2O(g)→N2(g)+IO(g)v=k1•c(N2O)•c(I)慢反应
第三步:IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)快反应12
其中可近似认为第二步反应不影响第一步的平衡。
实验表明,含碘时N2O分解速率方程v=k•c(N2O)•[c(I2)]0.5(k为速率常数)。
①k=(用含K和k1的代数式表示)。
②下列表述正确的是。
a.IO为反应的中间产物
b.碘蒸气的浓度大小不会影响N2O的分解速率
c.第二步对总反应速率起决定作用
d.催化剂会降低反应的活化能,从而影响ΔH
(4)通过N2O传感器可监测环境中N2O的含量,其工作原理如图所示。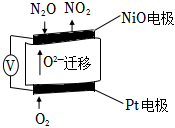
①NiO电极上的电极反应式为。
②N2O浓度越高,则电压表读数越(填“高“或“低“)。组卷:30引用:1难度:0.5


