2022-2023学年新疆和田地区民丰县高二(上)期中化学试卷
发布:2024/8/28 1:0:8
一、单项选择题:本题共10小题,每小题3分,共40分.每小题只有一个选项符合题意.
-
1.当前,废电池必须进行集中处理的问题已被提到议事日程,其首要原因是( )
组卷:6引用:2难度:0.9 -
2.下列有关化学反应速率和限度的说法中不正确的是( )
组卷:15引用:5难度:0.5 -
3.下列判断及叙述,正确的是( )
组卷:1引用:1难度:0.5 -
4.N2(g)+3H2(g)
2NH3(g)△H<0.向容器中通入1mol N2和3mol H2,当反应达到平衡时,下列措施能提高N2转化率的是( )催化剂高温高压
①降低温度;②维持温度、容积不变,按照物质的量之比为1:3再通入一定量的N2和H2;③增加N2的物质的量;④维持恒压条件,通入一定量惰性气体组卷:70引用:2难度:0.5 -
5.下列操作能实现相应目的的是( )
组卷:3引用:2难度:0.5
二、填空题:共计60分.
-
14.发射航天火箭常用肼(N2H4)与N2O4作燃料与助燃剂.
(1)肼易溶于水,性质与氨相似,用电离方程式表示肼的水溶液显碱性的原因.
(2)肼(N2H4)与N2O4的反应为:2N2H4 (1)+N2O4 (1)=3N2(g)+4H2O(1)ΔH=-1225kJ•mol-1
已知反应相关的化学键键能数据如下:
则使1mol N2O4 (1)分子中化学键完全断裂时需要吸收的能量是化学键 N-H N-N N≡N O-H E/(kJ•mol-1) 390 190 946 460
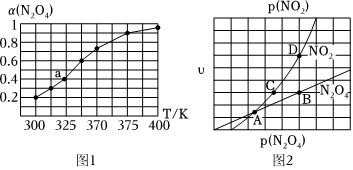
(3)N2O4与NO2之间存在反应N2O4(g)═2NO2(g).将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图1所示.
①由图推测该反应ΔH0(填“>”或“<”),理由为,若要提高N2O4的转化率,除改变反应温度外,其他措施有(要求写出一条).
②图中a点对应温度下,已知N2O4的起始压强p0为108kPa,列式计算该温度下反应的平衡常数Kp=(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
③在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系:υ(N2O4)=k1p(N2O4),υ(NO2)=k2p2(NO2),其中kl、k2是与反应温度有关的常数.相应的速率一压强关系如图2所示,一定温度下,kl、k2与平衡常数Kp的关系是kl=,在图标出的点中,能表示反应达到平衡状态的点为,理由是.组卷:14引用:2难度:0.5 -
15.按要求回答下列问题:
Ⅰ.肼(N2H4)与氧化剂N2O4(l)反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)═N2O4(l) ΔH1=-195kJ•mol-1
②N2H4(l)+O2(g)═N2(g)+2H2O(g) ΔH2=-534kJ•mol-1
(1)写出N2H4(l)和N2O4(l)完全反应生成N2和水蒸气的热化学方程式:。
Ⅱ.根据图填空:
(2)图1为含有少量Zn杂质的粗银电解精炼银的示意图,则:
①(填“a”或“b“)极为含有杂质的粗银。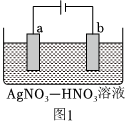
②电解一段时间后电解液中c(Ag+)浓度(填“偏大”、“偏小”或“不变”)。
③若b极有少量红棕色气体生成,则生成该气体的电极反应式为。
(3)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图2所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是。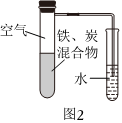
A.铁被氧化的电极反应式为Fe-2e-═Fe2+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀组卷:0引用:2难度:0.6


