2022-2023学年河北省张家口市高二(上)期末化学试卷
发布:2024/8/16 2:0:0
一、单项选择题:本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是符合题目要求的。
-
1.河北的钢铁业为中国的工业发展做出了不容忽视的贡献,获得了全国各界的关注和赞叹。钢铁的冶炼原理之一为3CO(g)+Fe2O3(s)⇌3CO2(g)+2Fe(s)ΔH<0。下列关于钢铁的生产、腐蚀和防护的说法错误的是( )
组卷:24引用:2难度:0.7 -
2.化学与生产、生活紧密相关,下列说法错误的是( )
组卷:6引用:2难度:0.5 -
3.近年来随着中国科技的崛起,中国电动汽车也随之获得迅猛发展。下列说法错误的是( )
组卷:11引用:2难度:0.7 -
4.25℃,101kPa下,关于反应2H2(g)+O2(g)═2H2O(g)ΔH═-483.6kJ⋅mol-1的相关叙述正确的是( )
组卷:72引用:2难度:0.7 -
5.二氧化硫的催化氧化反应:O2(g)+2SO2(g)⇌2SO3(g)ΔH<0是工业制硫酸中的重要反应。某温度下,在一密闭容器中探究二氧化硫的催化氧化反应,下列叙述正确的是( )
组卷:84引用:3难度:0.8
三、非选择题:本题共4小题,共57分。
-
16.绿矾(FeSO4•7H2O)是一种重要的化工原料。为检测某部分被氧化的绿矾中亚铁离子的质量分数设计如下实验。
步骤一:精确称量部分被氧化的绿矾5.000g,加入适量硫酸溶解并配制成250mL溶液。
步骤二:取所配溶液25.00mL于锥形瓶中,用0.0100mol•L-1KMnO4溶液滴定至终点。
步骤三:重复步骤二2~3次,平均消耗KMnO4溶液的体积为20.00mL。
(1)步骤一中需要用到下列仪器中的(填选项字母)。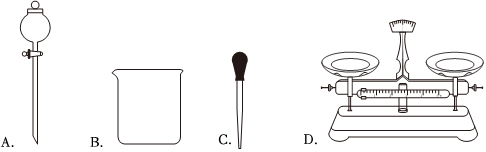
(2)步骤二中KMnO4溶液应用(填“酸式”或“碱式”)滴定管盛装。滴定时发生反应的离子方程式为。
(3)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):检漏→蒸馏水洗涤→()→()→()→()→()→开始滴定。
A.装入0.0100mol•L-1KMnO4溶液至零刻度以上
B.用0.0100mol•L-1KMnO4溶液润洗2至3次
C.排除气泡
D.记录起始读数
E.调整液面至零刻度或零刻度以下
(4)步骤二中滴定至终点时的实验现象为。
(5)被氧化的绿矾中亚铁离子的质量分数为;若滴定终点时仰视读数,则测得亚铁离子的质量分数(填“偏低”“偏高”或“不变”)。组卷:6引用:1难度:0.5 -
17.党的二十大在“推动绿色发展,促进人与自然和谐共生”中提到:积极稳妥推进碳达峰碳中和。CO2的资源化利用是实现“碳达峰碳中和”的重要途径。CO2合成甲醇的过程中涉及如下反应。
反应ⅰ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1
反应ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=+41.1kJ•mol-1
已知部分化学键键能如下表:
(1)ΔH1=化学键 C=O C-H H-O H-H C-O 键能/(kJ•mol-1) 754 403 459 446 309 。
(2)CO2合成甲醇的过程,增大压强,CO2的平衡体积分数(填“增大”“减小”或“无影响”),原因为。
(3)反应ⅱ的反应速率方程可表示为v正=k正c(CO2)•c(H2),v逆=k逆c(CO)•c(H2O),其中k正、k逆分别为正、逆速率常数,则升高温度k正会(填“增大”“减小”或“无影响”)。
(4)恒压下进行CO2合成甲醇实验。初始压强为100kPa,起始投料n(CO2)、n(H2)均为1mol,CO2和H2的平衡转化率随温度变化曲线如图所示。
①曲线(填“L1”或“L2”)表示CO2的平衡转化率。
②温度高于T2K后曲线L2随温度升高而降低的原因为。
③T1K下,反应达到平衡时,H2O(g)的物质的量n(H2O)=,反应ⅰ的标准平衡常数Kθ=(保留1位小数)(已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g)⇌gG(g)+hH(g),Kθ=,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压)。(pGpθ)g•(pHpθ)h(pDpθ)d•(pEpθ)e组卷:38引用:2难度:0.7


