2022-2023学年广东省广州三校(广附、铁一、广外)联考高一(下)期末化学试卷
发布:2024/7/20 8:0:8
一、选择题:本题共16小题,其中1-10题每题2分,11-16题每题4分,共44分。
-
1.能源危机是当前全球性的问题,“开源节流”是应对能源危机的重要举措。下列做法不利于能源“开源节流”的是( )
组卷:32引用:2难度:0.9 -
2.少量铁粉与100mL1.0mol⋅L-1的稀盐酸反应,为了加快此反应速率且不改变生成H2的总量,以下方法可行的是( )
①适当升高温度;
②再加入100mL1.0⋅mol⋅L-1的稀盐酸;
③滴入几滴硫酸铜溶液;
④加入少量醋酸钠固体;
⑤加几滴浓硫酸组卷:143引用:3难度:0.6 -
3.反应A+B→C(放热)分两步进行:①A+B→X(吸热),②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是( )
组卷:1034引用:62难度:0.9 -
4.如图是生活中常用的锌锰干电池的示意图,下列有关说法中不正确的是( )
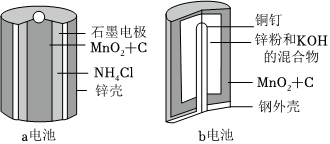 组卷:53引用:2难度:0.7
组卷:53引用:2难度:0.7 -
5.如图为实验室制取少量乙酸乙酯的装置图.下列关于该实验的叙述中,不正确的是( )
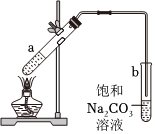 组卷:131引用:2难度:0.7
组卷:131引用:2难度:0.7 -
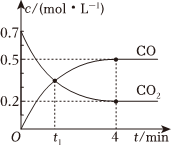 6.一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)⇌FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。下列说法正确的是( )组卷:58引用:6难度:0.7
6.一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)⇌FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。下列说法正确的是( )组卷:58引用:6难度:0.7
二、非选择题:本题共4道小题,共56分。
-
19.H2O2是一种常见试剂,在实验室、工业生产上有广泛用途
Ⅰ.H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。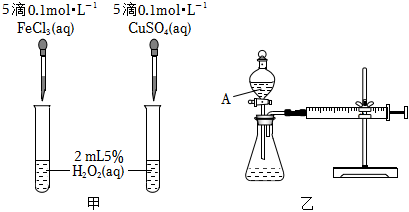
(1)若利用图甲装置,可通过观察现象,从而定性比较得出结论。
(2)有同学提出将0.1mol⋅L-1FeCl3改为mol⋅L-1Fe2(SO4)3更为合理,其理由是。
(3)若利用乙实验可进行定量分析,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是。
(4)如图为某小组研究的酸、碱对H2O2分解的影响。该小组提出可以用BaO2固体与H2SO4溶液反应制H2O2,反应的化学方程式为,支持这一方案的理由是。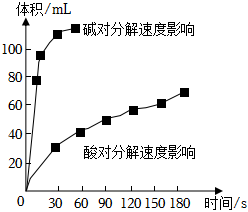
Ⅱ.实验室用H2O2快速制氧气,其分解速率受多种因素影响。实验测得70℃时不同条件下H2O2浓度随时间的变化如甲、乙、丙、丁四图所示: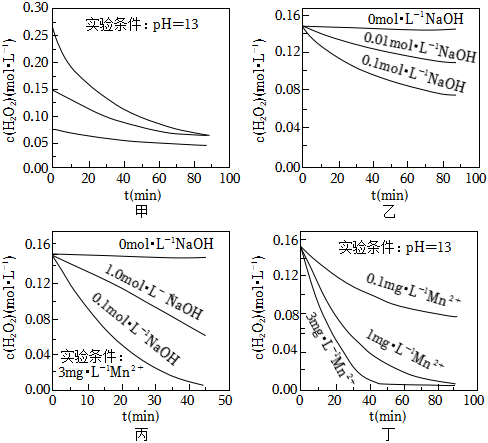
(5)下列说法正确的是:(填字母序号)。
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解越慢
B.图乙表明,其他条件相同时,溶液碱性越弱,H2O2分解越快
C.图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解越快
D.图丁表明,碱性溶液中,Mn2+浓度越大,对H2O2分解速率的影响越大
(6)催化剂Mn2+在反应中,改变了(填字母序号)。
A.反应速率
B.反应限度
C.反应焓变
D.反应路径
E.反应活化能
F.活化分子百分数组卷:96引用:1难度:0.5 -
20.电池的种类繁多,应用广泛,根据电化学原理回答下列问题:
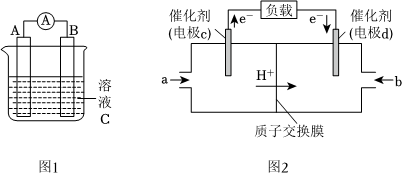
(1)图1中,若溶液C为稀H2SO4,电流表指针发生偏转,B电极材料为Zn且作负极,则A电极上发生的电极反应式为;反应进行一段时间后溶液酸性将(填“增强”“减弱”或“基本不变”)。
(2)C2H5OH可作为燃料使用,用C2H5OH和O2组合形成的质子交换膜燃料电池的结构示意图如图2,电池总反应为C2H5OH+3O2=2CO2+3H2O,则d电极是(填“正极”或“负极”),c电极的电极反应式为。若线路中转移4mol电子,则上述C2H5OH燃料电池消耗的O2在标准状况下的体积为L。
(3)一种熔融碳酸盐燃料电池的原理示意图如图。请回答下列问题: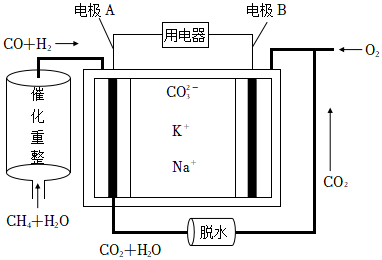
①反应CH4+H2O3H2+CO,每消耗1molCH4理论上转移的电子数目为催化剂△。
②电池工作时,向电极CO2-3(填“A”或“B”)移动。
③电极B上发生的电极反应为。
(4)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示: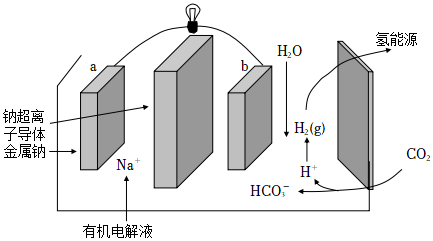
①系统工作时,a极为极,b极区的电极反应式为。
②系统工作时b极区有少量固体析出,可能的原因是。组卷:87引用:1难度:0.6


