2021-2022学年湖北省新高考高三(上)质检化学试卷(12月份)
发布:2024/9/16 0:0:8
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
-
1.我国古代劳动人民用“失蜡法”铸造青铜器:用蜂蜡作成铸件模型,再用黏土敷成外范,烧成陶模,烧制过程蜡模全部融化流失,使整个铸件模型变成空壳,再往内浇灌青铜熔液,便铸成器物。下列说法正确的是( )
组卷:2引用:1难度:0.7 -
2.合理的工业设计和能源利用是改善环境的重要手段。下列有关说法中错误的是( )
组卷:4引用:1难度:0.7 -
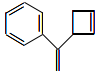 3.一种有机物的结构简式如图所示。下列关于该有机物的说法正确的是( )组卷:1引用:1难度:0.6
3.一种有机物的结构简式如图所示。下列关于该有机物的说法正确的是( )组卷:1引用:1难度:0.6 -
4.下列指定反应的离子方程式正确的是( )
组卷:1引用:1难度:0.5 -
5.下列实验操作不能达到实验目的的是( )
选项 操作及现象 实验目的 A 纯碱与5mol•L-1的硫酸反应后的气体直接通入硅酸钠溶液中,产生白色胶状沉淀 证明非金属性:C>Si B 淀粉酸性水解液中加入足量的NaOH溶液中和,然后滴加碘水,溶液未变蓝 确认淀粉已水解完全 C 向某无色溶液中加入铜片和稀硫酸,试管口有红棕色气体出现 无色溶液中存在 NO-3D 滴有酚酞的纯碱溶液中加入少量BaCl2固体,有白色沉淀生成,且溶液红色变浅 验证纯碱溶液存在水解平衡 组卷:0引用:1难度:0.7 -
6.NA为阿伏加德罗常数的数值。下列有关叙述错误的是( )
组卷:1引用:1难度:0.7
二、非选择题:本题包括4小题,共55分。
-
18.柳酸甲酯(
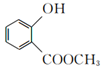 )常用于医药制剂的赋香剂,实验小组利用邻羟基苯甲酸(
)常用于医药制剂的赋香剂,实验小组利用邻羟基苯甲酸(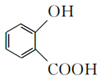 )和甲醇在浓硫酸催化下合成少量柳酸甲酯。
)和甲醇在浓硫酸催化下合成少量柳酸甲酯。
Ⅰ.实验原理: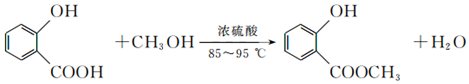
Ⅱ.相关数据如表:
Ⅲ.实验步骤:名称 分量 颜色状态 相对密度 熔点(℃) 沸点(℃) 溶解性(中) 柳酸甲酯 152 无色液体 1.18 -8.6 224 微溶 邻羟基苯甲酸 138 白色晶体 1.44 158 210 不溶 甲醇 32 无色液体 0.792 -97 64.7 互溶
合成:向A中加入6.9g邻羟基苯甲酸、适量固态酸性催化剂、24g甲醇,10mL甲苯(甲苯与能水形成的共沸物,沸点为85℃,易将水蒸出)加热回流1.5小时;
提纯:反应完毕,待装置冷却后,分离出固态催化剂,依次用水洗、5%的NaHCO3溶液洗、水洗,将产物移至干燥的烧杯中加入0.5g无水氯化钙,一段时间后,过滤,蒸馏有机层获得4.5g纯品。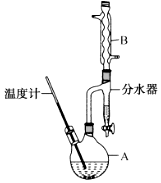
回答下列问题:
(1)甲苯蒸气、甲醇蒸气、水蒸气冷凝为液体,然后通过分水器,甲苯、甲醇重新流回到A中,打开活塞将水从下口放出。下列有关说法中错误的是(填字母)。
A.使用分水器能提高反应物的利用率
B.使用分水器能够促使反应正向进行
C.分水器中的水面不再变化时,反应达到最大限度
D.10mL甲苯也可用四氯化碳代替
(2)在提纯步骤中,一定没有用到下列仪器中的(填仪器名称)。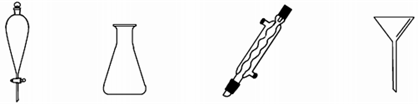
(3)提纯步骤中第二次水洗的目的是;无水氯化钙的作用是。
(4)本实验的产率为%(保留三位有效数字)。
(5)实验小组为了探究影响产率的因素,采集了如下数据(邻羟基苯甲酸易溶于甲醇):
①实验Ⅳ中x=编号 邻羟基苯甲酸/g 甲醇/mL 反应时间/min 催化剂用量/g 产率/% Ⅰ 4.8 4.0 8 1.4 61.67 Ⅱ 4.8 4.0 8 1.0 55.42 Ⅲ 4.8 5.0 8 1.4 65.42 Ⅳ 4.8 x 4 1.4 - ;设计实验Ⅳ是为了探究对产率的影响。
②增加甲醇的体积会提高产率,但甲醇超过一定量时,反应时间相同的情况下,产率反而下降,试从速率角度分析产率下降的主要原因:。组卷:7引用:1难度:0.5 -
19.丙烯是化工合成的重要原料,其制备工艺主要有如下两种:
工艺1:丙烷无氧脱氢工艺:C3H8(g)⇌C3H6(g)+H2(g)
工艺2:丙烷氧化脱氢工艺:2C3H8(g)+O2(g)⇌2C3H6(g)+2H2O(g)ΔH=-235kJ•mol-1
回答下列问题:
(1)根据下表数据,计算无氧脱氢工艺中的ΔH=kJ•mol-1,与工艺1相比,工艺2的优点是(从能源角度)。
(2)若提高工艺1丙烯的平衡转化率,下列措施不可行的是物质 C3H8(g) C3H6(g) H2(g) 燃烧热(kJ•mol-1) 2217.8 2058.0 285.8 (填字母)。
A.适当的升高温度
B.增大压强
C.提高恒容反应容器中丙烷的初始浓度
D.向恒压反应容器中的丙烷掺入水蒸气(水蒸气不参与反应)
(3)工艺1脱氢时以CeO2/VO3为催化剂,脱第1个氢原子的反应历程有两种情况(Ts表示过渡态):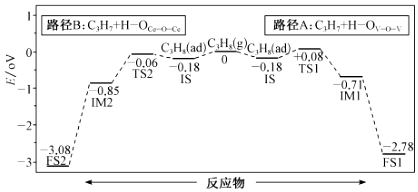
用图中数据可知,脱第1个氢原子时,最有可能按路径(填A或B),其原因是。
(4)工艺1脱氢时,还会产生副产物C2H4,写出生成副产物的化学方程式:,若恒容反应容器中C3H8(g)的浓度为5mol•L-1,丙烷的总平衡转化率为40%,丙烯的选择性为50%,则工艺1的平衡常数K=[结果保留两位有效数字,丙烯的选择性=×100%]。n(转化为丙烯消耗的丙烷)n(消耗的丙烷)组卷:1引用:1难度:0.5


