丙烯是化工合成的重要原料,其制备工艺主要有如下两种:
工艺1:丙烷无氧脱氢工艺:C3H8(g)⇌C3H6(g)+H2(g)
工艺2:丙烷氧化脱氢工艺:2C3H8(g)+O2(g)⇌2C3H6(g)+2H2O(g)ΔH=-235kJ•mol-1
回答下列问题:
(1)根据下表数据,计算无氧脱氢工艺中的ΔH=+126.0+126.0kJ•mol-1,与工艺1相比,工艺2的优点是 工艺2放热,能耗低等工艺2放热,能耗低等(从能源角度)。
| 物质 | C3H8(g) | C3H6(g) | H2(g) |
| 燃烧热(kJ•mol-1) | 2217.8 | 2058.0 | 285.8 |
BC
BC
(填字母)。A.适当的升高温度
B.增大压强
C.提高恒容反应容器中丙烷的初始浓度
D.向恒压反应容器中的丙烷掺入水蒸气(水蒸气不参与反应)
(3)工艺1脱氢时以CeO2/VO3为催化剂,脱第1个氢原子的反应历程有两种情况(Ts表示过渡态):
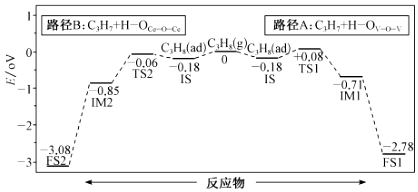
用图中数据可知,脱第1个氢原子时,最有可能按路径
B
B
(填A或B),其原因是 路径B的活化能低,反应速率快
路径B的活化能低,反应速率快
。(4)工艺1脱氢时,还会产生副产物C2H4,写出生成副产物的化学方程式:
2C3H8=3C2H4+2H2
2C3H8=3C2H4+2H2
,若恒容反应容器中C3H8(g)的浓度为5mol•L-1,丙烷的总平衡转化率为40%,丙烯的选择性为50%,则工艺1的平衡常数K=0.67
0.67
[结果保留两位有效数字,丙烯的选择性=n
(
转化为丙烯消耗的丙烷
)
n
(
消耗的丙烷
)
【答案】+126.0;工艺2放热,能耗低等;BC;B;路径B的活化能低,反应速率快;2C3H8=3C2H4+2H2;0.67
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/16 0:0:8组卷:1引用:1难度:0.5
相似题
-
1.氢气最早于16世纪被人工制取出来,氢气是一种清洁能源。
(1)利用光伏电池电解水制H2是氢能的重要来源。已知:H-H键、O=O键、H-O键的键能依次为436kJ•mol-1、495kJ•mol-1、463kJ•mol-1。则2H2O(g)═2H2(g)+O2(g)△H=kJ•mol-1。
(2)T1℃时,向5L恒容密闭容器中充入0.5molCH4,只发生反应2CH4(g)⇌C2H4(g)+2H2(g),达到平衡时,测得c(C2H4)=2c(CH4),CH4的转化率为;保持其他条件不变,温度改为T2℃,经25s后达到平衡,测得c(CH4)=2c(C2H4),则0~25s内v(C2H4)=mol•L-1•s-1。
(3)CH4分解时几种气体的平衡分压(pPa)的对数值lgp与温度的关系如图所示。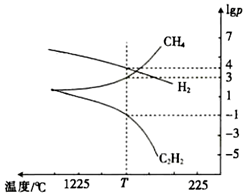
①T℃时,向一恒容密闭容器中通入一定量的CH4(g)、C2H4(g)和H2(g),只发生反应2CH4(g)⇌C2H2(g)+3H2(g)ΔH,ΔH(填“>”或“<”)0,此时的平衡常数Kp=(用平衡分压代替浓度进行计算)Pa2。
②若只改变一个反应条件使Kp变大,则该条件是(填标号)。
A.减小C2H2的浓度
B.升高温度
C.增大压强
D.加入合适的催化剂
(4)工业上,以KNH2和液氨为电解质,以石墨为电极,电解液氨制备H2。阳极的电极反应式为,一段时间后阴、阳两极收集到的气体质量之比为。发布:2025/1/4 8:0:1组卷:9引用:3难度:0.5 -
2.反应 4A(g)+5B(g)⇌4C(g)+6D(g)在 5L 的密闭容器中进行,半分钟后,C 的物质的量增 加了 0.30mol。下列叙述正确的是( )
发布:2024/12/30 19:30:2组卷:67引用:6难度:0.6 -
3.将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1mol/(L•min).求:
(1)此时A的浓度c(A)=mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)=mol;
(2)B的平均反应速率v(B)=mol/(L•min);
(3)x的值为.发布:2024/12/30 19:0:1组卷:163引用:26难度:0.3


