2022-2023学年四川省成都市高二(下)期末化学试卷(零诊)
发布:2024/7/18 8:0:9
一、本卷选择题共20小题。每小题2分,共40分。每小题只有一个选项符合题目要求。
-
1.关于下列物质应用的说法合理的是( )
组卷:9引用:1难度:0.7 -
2.下列物质分类正确的是( )
组卷:19引用:1难度:0.7 -
3.下列化学用语使用正确的是( )
组卷:15引用:1难度:0.8 -
4.NA代表阿伏加德罗常数的值。下列说法正确的是( )
组卷:53引用:1难度:0.7 -
5.下列转化不属于氧化还原反应的是( )
组卷:191引用:1难度:0.6 -
6.能正确表示下列化学变化的离子方程式是( )
组卷:40引用:1难度:0.7 -
7.下列实验现象描述正确的是( )
组卷:36引用:1难度:0.7 -
8.化学与生产、生活密切相关,下列应用与盐类水解无关的是( )
组卷:88引用:1难度:0.7
第II卷(非选择题,共60分)
-
25.我国是世界上最早制得和使用金属锌的国家。一种由菱锌矿(主要成分ZnCO3,含杂质FeCO3、MnCO3、MgO等)为原料制备金属锌的工艺流程如图:
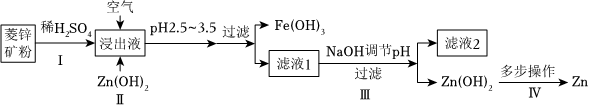
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题。金属离子 Zn2+ Fe2+ Mn2+ Mg2+ 开始沉淀时的pH 5.0 7.6 8.5 9.6 沉淀完全时(c=1.0×10-6mol•L-1)的pH 8.0 9.0 10.5 11.1
(1)步骤Ⅰ能够增加菱锌矿浸出率的方法有(写一条)。
(2)步骤Ⅱ中通入空气的目的是。
(3)根据上表数据,步骤Ⅲ应调节pH的范围是;Zn(OH)2的Ksp=。
(4)“滤液2”中除了Mn2+外,还含有的金属离子是。
(5)步骤Ⅳ的“多步操作”之一是用NaOH溶液将Zn(OH)2转化为Na2ZnO2,反应的化学方程式为。组卷:32引用:1难度:0.5 -
26.一氧化二氮可以用作火箭氧化剂,在室温下稳定,易于储存和飞行使用。现利用汽车尾气中的NO与H2反应来制备N2O气体,回答下列问题。
(1)已知:H2的燃烧热为286kJ•mol-1
①N2(g)+O2(g)=2NO(g) ΔH1=+180kJ•mol-1
②2N2(g)+O2(g)=2N2O(g) ΔH2=+164kJ•mol-1
③H2O(1)=H2O(g) ΔH3=+44kJ•mol-1
反应2NO(g)+H2(g)⇌N2O(g)+H2O(g)的ΔH=kJ•mol-1。
(2)总反应分为两步进行:
第①步:2NO(g)=N2O2(g)
第②步:。
实验发现,第①步反应几乎不影响总反应到达平衡所用的时间,由此推断,下列关于该反应叙述正确的是。(填序号)
A.更换催化剂,可改变反应的ΔH
B.步骤①的逆反应活化能一定小于②的
C.步骤②的有效碰撞频率小于步骤①
D.反应进程中N2O2属于中间产物
(3)在1093K时,NO与H2以物质的量之比为2:1混合置于某密闭容器中,在恒温恒压(100kPa)的条件下,发生反应2NO(g)+H2(g)⇌N2O(g)+H2O(g)。达到平衡时,测得N2O的体积分数为20%,NO的转化率为;该平衡的Kp=(以分压表示,分压=总压×物质的量分数)。
(4)既能提高NO的平衡转化率又能加快反应的速率,可采取的措施是。组卷:11引用:1难度:0.5


