2022-2023学年四川师大附中高二(上)月考化学试卷(12月份)
发布:2024/9/1 1:0:8
一、选择题(每题只有一个选项符合题意,每题2分共40分)
-
1.《科学》杂志评出“十大科技突破”,其中“火星上‘找’到水的影子”名列第一。下列关于水的说法正确的是( )
组卷:58引用:4难度:0.7 -
2.下列叙述中,不能用勒夏特列原理解释的是( )
组卷:3引用:1难度:0.5 -
3.NA为阿伏加德罗常数的值,下列说法正确的是( )
组卷:2引用:1难度:0.8 -
4.如图实验操作能达到实验目的的是( )
 组卷:16引用:5难度:0.5
组卷:16引用:5难度:0.5 -
5.下列各组离子一定能在指定环境中大量共存的是( )
组卷:4引用:1难度:0.5 -
6.在2L密闭恒容容器内,500℃时反应:2NO(g)+O2(g)⇌2NO2(g)的体系中,n(NO)随时间的变化如表(K表示平衡常数):
下列说法正确的是( )时间(s) 0 1 2 3 4 n (NO)(mol) 0.020 0.010 0.008 0.007 0.007 组卷:2引用:1难度:0.5 -
7.对于反应A(g)+3B(g)═2C(g)+2D(g),下列分别表示不同条件下的反应速率,则反应速率大小关系正确的是( )
①v(A)=0.01mol•L-1•s-1
②v(B)=1.20mol•L-1•min-1
③v(C)=2.40mol•L-1•min-1
④v(D)=0.03mol•L-1•s-1组卷:10引用:1难度:0.5 -
8.在某容积一定的密闭容器中,有下列的可逆反应:A(g)+B(g)⇌xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是( )
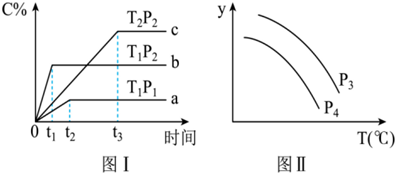 组卷:6引用:1难度:0.5
组卷:6引用:1难度:0.5 -
9.在恒容密闭容器中,将10 mol CO和一定量的H2S混合加热并达到下列平衡:CO(g)+H2S(g)⇌COS(g)+H2(g) K=1,平衡后CO物质的量为8 mol.下列说法正确的是( )
组卷:10引用:3难度:0.6
二、填空题,共60分
-
26.我国科学家研制的第二代“彩虹鱼”万米级深海着陆器所用的金属材料主要是钛合金。以钛铁矿(成分:FeTiO3及少量Fe2O3、FeO等杂质)为主要原料制钛的流程如图:
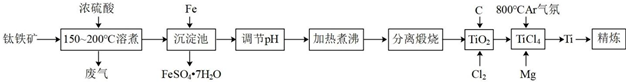
已知:①钛在常温下不与强酸、强碱反应;
②Ti4+易水解生成TiO2+,TiO2+进一步水解可得H2TiO3。
(1)“废气”中含有少量空气污染物,其分子式为。
(2)“150~200℃溶煮”时生成Ti(SO4)2和TiOSO4且有气体产生,写出生成TiOSO4反应的化学方程式。
(3)沉淀池中加入Fe时,开始无气泡,溶液由棕黄色变浅绿色,片刻后有无色无味气体产生。写出Fe参与的离子反应方程式。
(4)“加热煮沸”操作的主要目的是。
(5)简述“精炼”阶段,从Ti、Mg混合物获得Ti的实验方案是。组卷:4引用:1难度:0.4 -
27.在工业上常用CO与H2合成甲醇,热化学方程式为CO(g)+2H2(g)⇌CH3OH(g)△H=akJ•mol-1,回答下列问题,已知:
①O2(g)+CO(g)⇌CO2(g)△H=-283.0kJ•mol-112
②H2(g)+O2(g)⇌H2O(g)△H=-241.8kJ•mol-112
③CH3OH(g)+O2(g)⇌CO2(g)+2H2O(g)△H=-192.2kJ•mol-132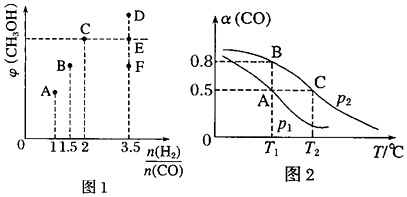
(1)a=。
(2)已知由CO2生成CO的化学方程式为CO2(g)+O(g)⇌CO(g)+O2(g),其正反应速率为v(正)=k(正)•c(CO2)•c(O),逆反应速率为v(逆)=k(逆)•c(CO)•c(O2),k为速率常数。2500K时,k(逆)=1.21×105L•s-1•mol-1,k(正)=3.02×105L•s-1•mol-1,则该温度下该反应的平衡常数K为。(保留小数点后一位小数)
(3)在T1时,向体积为2L的恒容容器中充入物质的量之和为3mol的CO和H2,发生反应CO(g)+2H2(g)⇌CH3OH(g),反应达到平衡时CH3OH(g)的体积分数(φ)与的关系如图1所示。n(H2)n(CO)
①对于反应CO(g)+2H2(g)⇌CH3OH(g),下列情况下一定达到化学平衡状态的是。
A.每断裂2mol H-H键同时断裂1mol O-H键
B.该反应的△H不再改变
C.在绝热恒容容器中反应至温度不再变化
D.2v(H2)正=v(CH3OH)逆
②当起始=2时,经过5min达到平衡,CO的转化率为0.6,则0~5min内平均反应速率v(H2)=n(H2)n(CO)。若此刻再向容器中加入CO(g)和CH3OH(g)各0.4mol,达到新平衡时H2的转化率将。(填“增大”、“减小”“或”“不变”)。
③当=3.5时,达到平衡后,CH3OH的体积分数可能是图象中的n(H2)n(CO)(填“D”“E”或“F”)点。
(4)在一容积可变的密闭容器中充有1mol CO和2mol H2,CO的平衡转化率(α)与温度(T)、压强(p)的关系如图2所示。
①A、B、C三点的平衡常数KA、KB、KC的大小关系为。
②若达到平衡状态A时,容器的体积为1L,则在平衡状态B时容器的体积为L。组卷:13引用:2难度:0.5


