2022-2023学年上海市闵行中学高二(下)期末化学试卷(等级考)
发布:2024/7/4 8:0:9
一、(本题20分,选择题为单选)
-
1.人们为了维持生命和健康,保证正常的生长发育和从事各种体力、脑力活动,每天必须从食物中摄取一定的营养素。其中糖类、油脂、蛋白质、维生素等是重要的有机营养素,它们有的参与新陈代谢,有的本身就是构成生命有机体重要的物质基础的生物大分子。请根据所学完成小题。
(1)央视纪录片《稻米之路》全面展示了“稻米”这种古老食物所走过的奇妙之旅。下列有关说法不正确的是。
A.淀粉属于糖类,但没有甜味
B.淀粉是天然高分子化合物
C.淀粉在人体内水解最终生成葡萄糖
D.大米中所含的主要营养物质是纤维素
为检验淀粉水解的情况,进行如图所示的实验,试管甲和丙均用60~80℃的水浴加热5~6min,试管乙不加热。待试管甲中的溶液冷却后再进行后续实验。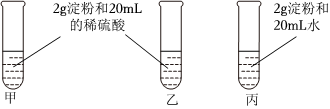
实验1:取少量甲中溶液,加入新制氢氧化铜,加热,没有砖红色沉淀出现。
实验2:取少量乙中溶液,滴加几滴碘水,溶液变为蓝色,但取少量甲中溶液做此实验时,溶液不变蓝色。
实验3:取少量丙中溶液加入NaOH溶液调节至碱性,再滴加碘水,溶液颜色无明显变化。
(2)写出淀粉水解的化学方程式:。
(3)设计甲和乙是为了探究对淀粉水解的影响,设计甲和丙是为了探究对淀粉水解的影响。
(4)实验1失败的原因是。
(5)实验3中溶液的颜色无明显变化的原因是。
(6)下列结论合理的是。
①淀粉水解需要在催化剂和一定温度下进行;
②欲检验淀粉是否完全水解,最好在冷却后的水解液中直接加碘;
③欲检验淀粉的水解产物具有还原性,应先在水解液中加入氢氧化钠中和硫酸至溶液呈碱性,再加入新制氢氧化铜并加热;
④若用唾液代替稀硫酸,则实验1可能出现预期的现象。
A.仅①②
B.仅③④
C.仅②③
D.①②③④均合理
(7)某油脂A的结构简式为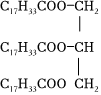 。从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是 (写结构简式)。
。从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是 (写结构简式)。
(8)蛋白质是生命的物质基础,是生命活动的主要承担者。绝大多数酶是蛋白质,因而具有蛋白质的特性;酶又是生物体内的催化剂,能在许多有机反应中发挥作用。在下面表示温度T与反应速率v之间关系的曲线中,有酶参加的是。
A.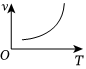 B.
B.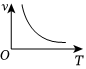 C.
C.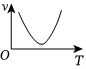 D.
D.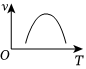
(9)由下列结构片段组成的蛋白质在胃液中水解,不可能产生的氨基酸是。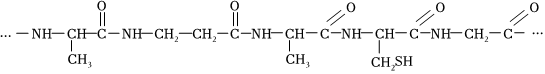
A.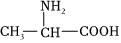 B.H2NCH2COOHC.
B.H2NCH2COOHC.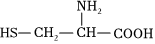 D.
D.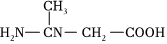
(10)因为核酸是生命的基础物质,是病毒的“身份证”,所以患者的确诊需要病毒的核酸检验。以下关于核酸的论述正确的是。
A.核酸是核蛋白的非蛋白部分,也是由氨基酸残基组成的
B.核酸水解产物中含有磷酸、葡萄糖和碱基
C.核酸、核苷酸都是高分子化合物
D.核酸有核糖核酸和脱氧核糖核酸两类,对蛋白质的合成和生物遗传起重要作用组卷:63引用:1难度:0.5
二、(本题22分,选择题为单选)
-
2.生活生产中的化学反应都伴随能量变化,要从物质和能量两个角度认识化学反应。根据有关知识完成小题。
(1)“即热饭盒”给人们生活带来方便,它可利用下面反应释放的热量加热食物。
A.生石灰和水
B.浓硫酸和水
C.纯碱和水
D.食盐和白醋
(2)下列反应中,属于吸热反应的是。
A.Na2O与水反应
B.铝和氧化铁反应
C.CaCO3受热分解
D.锌与盐酸反应
(3)将20gBa(OH)2•8H2O晶体与10gNH4Cl晶体一起放入烧杯中,用玻璃棒快速搅拌,用手触摸烧杯底部感觉,同时闻到气味。说明Ba(OH)2•8H2O跟NH4Cl的反应是(填“吸热”或“放热”)反应。该反应的化学方程式。
(4)NaOH稀溶液跟稀盐酸反应的中和热与KOH稀溶液跟稀硫酸反应的中和热(填“相等”或“不等”),原因是(用适当的文字和离子方程式解释)。组卷:49引用:1难度:0.5
-
3.获取能量变化有多种途径和方法,请根据所学完成下列各题。
(1)通过化学键的键能计算。已知:
则2H2(g)+O2(g)═2H2O(g) ΔH=化学键 H-H O-O O-H 键能(kJ•mol-1) 436 496 463.4 kJ⋅mol-1。
(2)通过物质所含能量计算。已知反应A+B=C+D中A、B、C、D所其存的能量依次可表示为EA、EB、EC、ED,该反应ΔH=。
(3)通过盖斯定律计算。已知在25℃、101kPa时,
2Na(s)+O2(g)═Na2O(s) ΔH1=-414kJ⋅mol-112
2Na(s)+O2(g)═Na2O2(s) ΔH2=-511kJ⋅mol-1
写出Na2O2与Na这应生成Na2O的热化学方程式:。
(4)利用实验装置测量,测量盐酸与NaOH溶液反应的热量变化的过程中,若取50mL0.50mol⋅L-1的盐酸,则还需加入。
A.50mL0.50mol⋅L-1NaOH溶液
B.50mL0.55mol⋅L-1NaOH溶液
C.1.0gNaOH固体
D.含0.025molNaOH的稀溶液组卷:22引用:1难度:0.5
五、(本题20分,选择题为单选)
-
12.合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(Ⅰ)溶液来吸收原料气中的CO,其反应是Cu(NH3)2Ac(aq)+CO(g)⇌[Cu (NH)3]2+Ac•CO(aq)。结合题干信息,完成各题。
(1)必须除去原料气中CO的原因为。
(2)醋酸二氨合铜(I)溶液吸收CO的生产适宜条件应为。
A.低温高压
B.低温低压
C.高温高压
D.高温低压
(3)吸收CO后的醋酸二氨合铜溶液经过适当处理又可再生,恢复其吸收CO的能力以供循环使用。醋酸二氨合铜溶液再生的生产适宜条件应是。
A.低温高压
B.低温低压
C.高温高压
D.高温低压组卷:16引用:1难度:0.7 -
13.有人设计了如图装置模拟工业合成氨(图中夹持装置均已略去)。
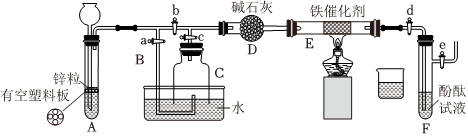
[实验操作]
①检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗注入一定量稀硫酸。打开弹簧夹c、d、e,则A中有氢气发生。在F出口处收集氢气并检验其纯度。
②关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③用酒精灯加热反应管E,继续通氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
回答下列问题:
(1)检验氢气纯度的目的是。
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是,防止了实验装置中压强过大。C瓶内气体的成分是。
(3)在步骤③中,先加热铁催化剂的原因是。组卷:28引用:2难度:0.7


