2022-2023学年上海市青浦高中高二(下)期末化学试卷
发布:2024/7/14 8:0:9
元素周期表中的秘密
-
1.元素周期律是对元素性质的规律性总结,元素周期表是这种规律的呈现形式。利用元素周期律可以推测一些未知元素可能的性质。根据你所学的周期律,回答下列问题:
(1)元素周期表有个周期,个主族。
A.6,7
B.7,7
C.7,18
D.7,14
(2)22Ti被誉为21世纪明星金属,其最外层电子数为。
A.1个
B.2个
C.3个
D.5个
(3)元素周期表中,第三电子层有一个未成对电子的元素有种。
A.2
B.3
C.4
D.5
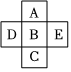
(4)如图所示,元素B与元素A之间的原子序数差值不可能为(同周期原子序数连续的元素视为相邻元素)。
A.2
B.8
C.18
D.32
上图中,所有元素最外层电子数之和为20,且D的最外层电子数为A原子序数的一半,回答下列问题:
(5)根据“对角线”相似原则,与D性质相似的元素(填元素符号,下同)。
(6)五种元素中能形成化合物种类最多的为,简述其原因。
(7)用一个方程式证明A的非金属性大于B。
三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器中得到广泛应用。NF3的键角为102°,其沸点为-129℃,可在铜的催化作用U下由F2和过量NH3反应得到。
(8)根据VSEPR理论计算可知。NF3的理想模型为形,实际为形。
(9)NF3的沸点比NH3的点(-33℃)低得多的主要原因是。
(10)简述NF3的键角为102°而不是109°28′的原因。
根据下表五种元素第一至第四电离能数据(单位:kJ⋅mol-1),回答下面各题:
(11)在周期表中,最可能处于同一族的是元素 I1 I2 I3 I4 Q 2080 4000 6100 9400 R 500 4600 6900 9500 S 740 1500 7700 10500 T 580 1800 2700 11600 U 420 3100 4400 5900 。
(12)T元素最多可能是区元素。若T为第二周期元素,F是第三周期元素中原子半径最小的元素,则T、F形成化合物其中心原子的杂化方式为。组卷:43引用:1难度:0.5
解答题
-
3.天然气的主要成分为甲烷,甲烷是最简单的烃,其结构为正四面体形,键角为109°28′,常温下为气态,能燃烧提供热量,是重要的生活生产的原料。
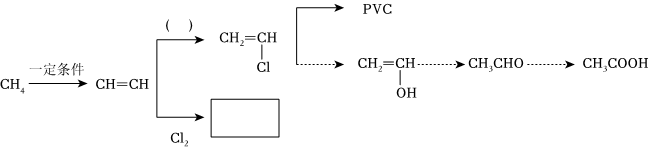
上述流程是以甲烷为原料进行的一系列有机合成,回答下列问题:
(1)完全燃烧8g甲烷、产生液态水和二氧化碳,同时放出445kJ的热量,写出热化学方程式。
(2)同温同压下,乙炔与氯气按(填比例)反应时,能生成一种具有顺反异构的产物。写出这两种顺反异构体。
(3)PVC是聚氯乙烯的简称,关于PVC的说法中正确的是。
A.属于混合物
B.不支持燃烧
C.用于制造食品包装袋
D.能使溴水褪色
(4)CH3COOH在一定条件下可以与Cl2发生α取代反应,生成2-氯乙酸,官能团名称;相同条件下,2-氯乙酸酸性比乙酸(填“强”或“弱”),简述理由。
(5)下列有机物的系统命名正确的是。
A.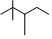 2,2,3-三甲基戊烷
2,2,3-三甲基戊烷
B.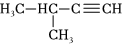 2-甲基-3-丁炔
2-甲基-3-丁炔
C.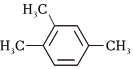 1,3,4-三甲苯
1,3,4-三甲苯
D.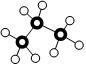 2,2-二甲基戊烷
2,2-二甲基戊烷
(6)有甲、乙、丙、丁、戊五支试管,均盛有溴水。在每支试管中加入足量下面一种试剂:①苯(ρ=0.88g⋅cm-3);②CCl4;③NaOH溶液;④酒精;⑤己烯,充分振荡后静置,其现象如图(图中阴影代表溶液有颜色)所示: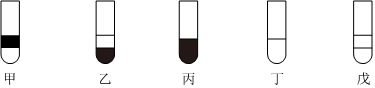
则甲、乙、丙、丁、戊五支试管中所加试剂依次排列顺序正确的是。
A.①③②④⑤
B.①②④⑤③
C.①②④③⑤
D.②①④⑤③
常温常压下,某气态烃7.2克在足量氧气中完全燃烧,生成CO2折合成S.T.P.状态下为11.2L,试回答下列问题:
(7)根据上述数据,该气态烃的最简式(实验式)为。
(8)甲同学认为,若要从最简式推断出分子式,必须要知道该分子的相对分子质量,以下数据无法替代或得出相对分子质量的是。
A.该烃折合成S.T.P.状态下的密度
B.同温同压下该烃相对于某气体的密度
C.该烃分子中的碳氢质量比
D.该烃分子中碳原子的数目
(9)乙同学认为该题不需要额外数据也能计算出结果,写出该烃的结构简式并命名。组卷:25引用:1难度:0.5
解答题
-
4.“氢分子沐足机”养生骗局:2022年央视曾曝光一起:“氢分子沐足机”养生骗局。商家称该机器能帮助身体排毒,并生成氢气抗衰老。将机器接通电源,观察到有气泡生成,机器底部不断产生红色的“毒素”沉淀。为了探究该机器的原理,某科学实验小组进行了探究:
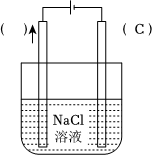
(1)该科学小组采用原子发射光谱法确定了气体为氢气。以下现象与原子发射光谱原理相同的是。
A.焰色试验
B.白光透过光栅时产生不同颜色的光
C.滴定管液面处蓝线粗细不同
(2)该科学小组采用了X射线射法确定所谓“毒素”其实是Fe2O3。有关X射线衍射法,下列说法不正确的是。
A.X射线衍射法可以确定晶胞大小和形状
B.X射线衍射法可以确定晶胞中的原子种类
C.X射线衍射法可以确定晶胞中原子的位置排列
D.X射线衍射法可能会损伤样品
(3)该科学小组还利用化学方法辅助鉴定毒素成分以确定毒素确为Fe2O3。取少量“毒素”样品,加入稀盐酸溶解,和KSCN溶液,出现血红色,证明毒素样品中含Fe3+,请写出溶液变为血红色的离子反应方程式。
(4)除KSCN溶液外,还可以使用亚铁氰化钾{K4[Fe(CN)6]}溶液鉴别Fe3+,现象为生成蓝色沉淀(KFeFe(CN)6)。K4[Fe(CN)6]可由向FeCl2溶液中加入KCN溶液制得。该反应开始时生成白色沉淀Fe(CN)2,后白色沉淀溶解并析出晶体K4[Fe(CN)6],请写出白色沉淀溶解析出晶体的离子方程式。
(5)K4[Fe(CN)6]是一种配位化合物,其配位数及配离子的空间构型为。
A.2,直线形
B.3,平面三角形
C.4,四面体形
D.6,八面体形
(6)KFeFe(CN)6判断化合物中第一个Fe的化合价。
A.0价
B.+2
C.+3
D.+6
(7)K4[Fe(CN)6]中,除了配位键外还存在键和键。
(8)若向(3)中血红色溶液中加入KCN溶液,会观察到血红色褪去,生成[Fe(CN)6]3-。请从配位键的强弱与离子反应发生条件角度说明为何该反应可以发生。
(9)经检测,该装置其实是一个电解装置,使用时,先向水中加入一勺食盐。请根据毒素成分及生成氢气,阴极材料选择惰性电极,阳极材料可选择。
(10)该装置的阳极反应为。
(11)NaCl没有参与反应,请分析NaCl在整个装置中起到的作用。
(12)沐足机在使用过程中,铁质把手容易生锈。请提出一条缓解把手生锈的建议。
(13)该沐足机在维修时,内部电路正负极接反了,会造成严重的安全隐患,请结合方程式和文字描述可能出现的隐患。组卷:26引用:1难度:0.7


