天然气的主要成分为甲烷,甲烷是最简单的烃,其结构为正四面体形,键角为109°28′,常温下为气态,能燃烧提供热量,是重要的生活生产的原料。
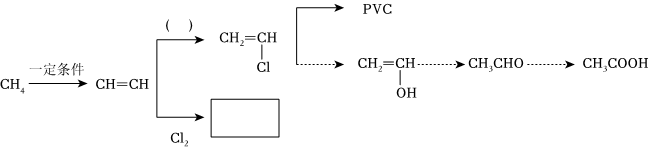
上述流程是以甲烷为原料进行的一系列有机合成,回答下列问题:
(1)完全燃烧8g甲烷、产生液态水和二氧化碳,同时放出445kJ的热量,写出热化学方程式 CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1。
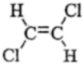
(2)同温同压下,乙炔与氯气按 1:11:1(填比例)反应时,能生成一种具有顺反异构的产物。写出这两种顺反异构体 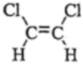 、
、
 、
、 。
。
(3)PVC是聚氯乙烯的简称,关于PVC的说法中正确的是 AA。
A.属于混合物
B.不支持燃烧
C.用于制造食品包装袋
D.能使溴水褪色
(4)CH3COOH在一定条件下可以与Cl2发生α取代反应,生成2-氯乙酸,官能团名称 碳氯键、羧基碳氯键、羧基;相同条件下,2-氯乙酸酸性比乙酸 强强(填“强”或“弱”),简述理由 电负性:Cl>H,C-Cl的极性大于C-H,导致氯乙酸羧基中羟基的极性更大,羟基更易电离出H+电负性:Cl>H,C-Cl的极性大于C-H,导致氯乙酸羧基中羟基的极性更大,羟基更易电离出H+。
(5)下列有机物的系统命名正确的是 AA。
A.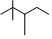 2,2,3-三甲基戊烷
2,2,3-三甲基戊烷
B.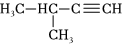 2-甲基-3-丁炔
2-甲基-3-丁炔
C.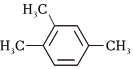 1,3,4-三甲苯
1,3,4-三甲苯
D.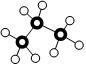 2,2-二甲基戊烷
2,2-二甲基戊烷
(6)有甲、乙、丙、丁、戊五支试管,均盛有溴水。在每支试管中加入足量下面一种试剂:①苯(ρ=0.88g⋅cm-3);②CCl4;③NaOH溶液;④酒精;⑤己烯,充分振荡后静置,其现象如图(图中阴影代表溶液有颜色)所示:
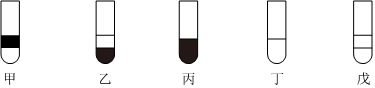
则甲、乙、丙、丁、戊五支试管中所加试剂依次排列顺序正确的是 CC。
A.①③②④⑤
B.①②④⑤③
C.①②④③⑤
D.②①④⑤③
常温常压下,某气态烃7.2克在足量氧气中完全燃烧,生成CO2折合成S.T.P.状态下为11.2L,试回答下列问题:
(7)根据上述数据,该气态烃的最简式(实验式)为 C5H12C5H12。
(8)甲同学认为,若要从最简式推断出分子式,必须要知道该分子的相对分子质量,以下数据无法替代或得出相对分子质量的是 CC。
A.该烃折合成S.T.P.状态下的密度
B.同温同压下该烃相对于某气体的密度
C.该烃分子中的碳氢质量比
D.该烃分子中碳原子的数目
(9)乙同学认为该题不需要额外数据也能计算出结果,写出该烃的结构简式并命名 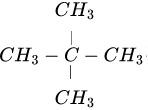 2,2-二甲基丙烷
2,2-二甲基丙烷 2,2-二甲基丙烷。
2,2-二甲基丙烷。
 、
、
 、
、
 2,2-二甲基丙烷
2,2-二甲基丙烷 2,2-二甲基丙烷
2,2-二甲基丙烷【答案】CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1;1:1; 、
、 ;A;碳氯键、羧基;强;电负性:Cl>H,C-Cl的极性大于C-H,导致氯乙酸羧基中羟基的极性更大,羟基更易电离出H+;A;C;C5H12;C;
;A;碳氯键、羧基;强;电负性:Cl>H,C-Cl的极性大于C-H,导致氯乙酸羧基中羟基的极性更大,羟基更易电离出H+;A;C;C5H12;C; 2,2-二甲基丙烷
2,2-二甲基丙烷
 、
、 ;A;碳氯键、羧基;强;电负性:Cl>H,C-Cl的极性大于C-H,导致氯乙酸羧基中羟基的极性更大,羟基更易电离出H+;A;C;C5H12;C;
;A;碳氯键、羧基;强;电负性:Cl>H,C-Cl的极性大于C-H,导致氯乙酸羧基中羟基的极性更大,羟基更易电离出H+;A;C;C5H12;C; 2,2-二甲基丙烷
2,2-二甲基丙烷【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/13 8:0:9组卷:25引用:1难度:0.5
相似题
-
1.肼(N2H4)可作为发射火箭的燃料。已知1g液态肼(N2H4)气体在空气中燃烧生成氮气和水蒸气,放出16.7kJ的热量,该反应的热化学方程式是( )
发布:2024/12/30 3:0:4组卷:124引用:9难度:0.6 -
2.氢在地球上主要以化合态的形式存在,是宇宙中分布最广泛的物质,它构成了宇宙质量的75%,属于二次能源.工业上生产氢的方式很多,常见的有水电解制氢,煤炭气化制氢,重油及天然气水蒸气催化制氢等.氢气是一种理想的绿色能源,如图1为氢能产生和利用的途径:
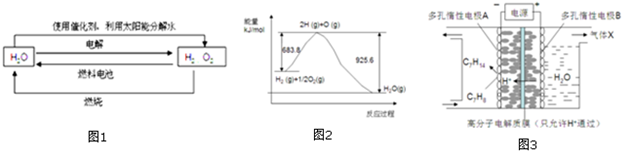
(1)图1的四个过程中能量转化形式有
A.2种 B.3种 C.4种 D.4种以上
(2)电解过程要消耗大量的电能,而使用微生物作催化剂在阳光下也能分解水.
2H2O(1)2H2(g)+O2(g)△H 1 2H2O(1)通电2H2(g)+O2(g)△H2光照催化剂
以上反应的△H1△H2(选填“<”、“>”或“=”)
(3)已知H2O(l)→H2O(g)△H=+44kJ.mol-1,依据图2能量变化写出氢气燃烧生产液态水的热化学方程式
(4)氢能利用需要选择合适的储氢材料.
①NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,且反应前后B的化合价不变,该反应的化学方程式为
②镧镍合金在一定条件下可吸收氢气生产氢化物:LaNi3(s)+3H2(g)═LaNi3H6(s)△H<0,欲使LaNi3H6(s)释放出气态氢,根据平衡移动的原理,可改变的条件之一是
③一定条件下,如图3所示装置可实现有机物的电化学储氢,使C7H8转化为C7H14,则电解过程中产生的气体X 为,电极A上发生的电极反应式为.发布:2024/12/17 8:0:2组卷:38引用:1难度:0.5 -
3.在298K、1.01×105Pa下,将0.5mol CO2通入750mL 1mol•L-1NaOH溶液中充分反应,测得反应放出xkJ的热量。已知在该条件下,1mol CO2通入1L 2mol•L-1NaOH溶液中充分反应放出ykJ的热量,则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
发布:2024/12/30 4:0:1组卷:145引用:5难度:0.7


